
【题目】有关NaHCO3和Na2CO3的下列叙述中错误的是( )
①等质量的NaHCO3和Na2CO3分别与足量盐酸反应,Na2CO3产生的CO2多
②84 g NaHCO3、106 g Na2CO3分别与足量的盐酸完全反应,Na2CO3消耗盐酸的物质的量是NaHCO3的两倍
③将澄清石灰水分别倒入两种盐溶液中,只有Na2CO3溶液中产生白色沉淀
④通常状况下,相同温度下,Na2CO3的溶解度大于NaHCO3
A. ①② B. ②③ C. ②④ D. ①③
【答案】D
【解析】①Na2CO3+2HCl![]() 2NaCl+H2O+CO2↑,NaHCO3+HCl
2NaCl+H2O+CO2↑,NaHCO3+HCl![]() NaCl+H2O+CO2↑,等质量的NaHCO3和Na2CO3分别与足量盐酸反应,NaHCO3产生的CO2多,故①错误;②Na2CO3+2HCl
NaCl+H2O+CO2↑,等质量的NaHCO3和Na2CO3分别与足量盐酸反应,NaHCO3产生的CO2多,故①错误;②Na2CO3+2HCl![]() 2NaCl+H2O+CO2↑,NaHCO3+HCl
2NaCl+H2O+CO2↑,NaHCO3+HCl![]() NaCl+H2O+CO2↑,84g即1molNaHCO3、106g即1molNa2CO3分别与足量的盐酸完全反应,Na2CO3消耗盐酸的物质的量是NaHCO3的两倍,故②正确;③将澄清石灰水分别倒入两种盐溶液中,Na2CO3+Ca(OH)2
NaCl+H2O+CO2↑,84g即1molNaHCO3、106g即1molNa2CO3分别与足量的盐酸完全反应,Na2CO3消耗盐酸的物质的量是NaHCO3的两倍,故②正确;③将澄清石灰水分别倒入两种盐溶液中,Na2CO3+Ca(OH)2![]() CaCO3↓+2NaOH,NaHCO3+Ca(OH)2
CaCO3↓+2NaOH,NaHCO3+Ca(OH)2![]() CaCO3↓+H2O+NaOH或2NaHCO3+Ca(OH)2
CaCO3↓+H2O+NaOH或2NaHCO3+Ca(OH)2![]() CaCO3↓+2H2O+Na2CO3,都产生白色沉淀,故③错误;④通常状况下,相同温度下,Na2CO3的溶解度大于NaHCO3,故④正确。故选D。
CaCO3↓+2H2O+Na2CO3,都产生白色沉淀,故③错误;④通常状况下,相同温度下,Na2CO3的溶解度大于NaHCO3,故④正确。故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在mA+nB===pC的反应中,m、n、p为各物质的系数,现测得C每分钟增加a mol·L-1,B每分钟减少1.5a mol·L-1,A每分钟减少0.5a mol·L-1,则m∶n∶p为
A.2∶3∶2 B.2∶2∶3
C.1∶3∶2 D.3∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅱ]丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+![]() O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=242 kJ·mol1
O2(g)= H2O(g) ΔH3=242 kJ·mol1
反应①的ΔH1为________kJ·mol1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是_________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
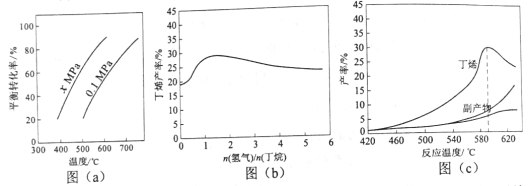
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是__________________________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅰ节选]近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
H2S与CO2在高温下发生反应:H2S(g)+CO2(g)![]() COS(g) +H2O(g)。在610 K时,将0.10 mol CO2
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2
与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率![]() =_______%,反应平衡常数K=________。
=_______%,反应平衡常数K=________。
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率![]() _____
_____![]() ,该反应的
,该反应的![]() H_____0。(填“>”“<”或“=”)
H_____0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是________(填标号)
A.H2S B.CO2 C.COS D.N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列排列顺序正确的是( )
A. 微粒半径:Mg2+>F- B. 稳定性:HI>HBr
C. 熔点:Al>Na D. 酸性:H2SO4>HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室制取蒸馏水的装置(如下图)中:

(1) 仪器A的名称是______________________温度计的水银球应位于______________________,
(2) 烧瓶中应放几粒沸石(或碎瓷片),其作用是_______________________________________,
(3) 冷凝管中冷凝水的流向应从______________(填“a”或“b”)口进。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠和铝均是重要的金属。
(1) 铝的原子结构示意图是___________________。
(2) 铝与NaOH溶液反应的离子方程式为______________________________;
(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为______________。
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工业合成氨反应 N2(g)+3H2(g) ![]() 2NH3 (g),以下分析不正确的是
2NH3 (g),以下分析不正确的是
A. 在5L固定容积的密闭容器内,前2分钟消耗2molN2,则v(N2)=0.2mol·L-1·min-1
B. 改变条件可使H2的转化率达100%
C. 每消耗3molH2,必然生成2molNH3
D. 合成氨是人类科学史上的一项重大突破,缓解了粮食不足问题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com