
【题目】(1)为除去CuSO4溶液中少量的Fe3+杂质,可加入某物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3而除去,调整溶液pH可选用下列物质中的________。
A. NaOH B. Cu C. Cu(OH)2 D. NH3·H2O
(2)在恒温、恒容条件下,将1molA和2molB充入一个密闭容器中,在一定条件下发生反应:A(g)+2B(g)![]() xC(g),达到平衡时,测得C的物质的量分数为m%;若开始充入容器中的是0.3mol A、0.6mol B和1.4mol C,达平衡时C的物质的量分数仍为m%,则x的值为_________________ 。
xC(g),达到平衡时,测得C的物质的量分数为m%;若开始充入容器中的是0.3mol A、0.6mol B和1.4mol C,达平衡时C的物质的量分数仍为m%,则x的值为_________________ 。
(3)25℃时,物质的量浓度相同的下列六种溶液:①NH3·H2O ②NH4HSO4 ③(NH4)2CO3 ④NH4Cl ⑤NH4Al(SO4)2 ⑥(NH4)2SO4 ,其中c(NH4+)从大到小的排列顺序为______________(填序号)。
(4)已知下列四组溶液中:①Na2S ② H2S 和NaHS ③H2S ④NaHS ,每种溶质的物质的量浓度均为0.4 mol·L-1,回答下列问题:
c(H2S)从大到小的顺序为____________________________(填序号)
c(S2-)从大到小的顺序为_____________________________(填序号)
【答案】 C 2或3 ⑥>③>②>⑤>④>① ②>③>④>① ①>④>②>③
【解析】(1)调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,则加含铜元素的物质与氢离子反应促进铁离子水解转化为沉淀,则C符合,A、D将铜离子转化为沉淀,不符合,B中Cu与Fe3+反应生成了Fe2+,引入了新杂质,不符合,故答案为: C;
(2)恒温恒容下,开始充入2molA和1molB与开始充入0.6molA、0.3molB和1.4molC达到平衡后,C的体积分数为m%,说明为完全等效平衡,按化学计量数转化到左边,满足n(A)=2mol、n(B)=1mol,故0.6mol+![]() =2mol,解得x=2,但是对于反应前后气体系数和相等的反应,物质的投料等比即等效,所以x=3也是正确的,故答案为:2或3;
=2mol,解得x=2,但是对于反应前后气体系数和相等的反应,物质的投料等比即等效,所以x=3也是正确的,故答案为:2或3;
(3)设物质的量浓度聚为1mol/L。①NH3·H2O为弱碱,电离程度很小,c(NH4+)很小;②④⑤三者中c(NH4+)都约为1mol/L,④NH4Cl中氯离子对铵根离子的水解无影响;②NH4HSO4中氢离子抑制铵根离子的水解;⑤NH4Al(SO4)2中铝离子的水解抑制铵根离子的水解,但抑制程度小于②;则c(NH4+)②>⑤>④;③⑥二者c(NH4+)都约为2mol/L,③(NH4)2CO3中碳酸根离子的水解促进铵根离子的水解;⑥(NH4)2SO4中硫酸根离子对铵根离子的水解无影响,则c(NH4+)⑥>③,因此c(NH4+)从大到小的排列顺序为⑥>③>②>⑤>④>①,故答案为:⑥>③>②>⑤>④>①;
(4)③H2S、②H2S和NaHS中存在大量硫化氢分子,且硫化氢的电离程度越大,则硫化氢浓度越小,则硫化氢浓度大小为:③<②; ④NaHS、①Na2S二者溶液中硫化氢浓度减小,硫氢根离子水解生成硫化氢,则②中数据生成的硫化氢浓度大于③,所以四种溶液中硫化氢浓度大小为:②>③>④>①;①Na2S中S2-水解程度较小,c(S2-)≈c(Na2S),最大;③H2S中S2-为二级电离产生的,电离程度非常小,c(S2-)最小;②④中S2-为NaHS电离产生的,但②中H2S和NaHS溶液的酸性比④大,抑制NaHS的电离,c(S2-):④>②,故四种溶液的c(S2-)从大到小的顺序为:①>④>②>③;故答案为:②>③>④>①;①>④>②>③。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】Na2CO3、NaHCO3是生活在常见的盐,某实验小组通过以下实验了探究这两种物质的性质(已知:Na2CO3、NaHCO3的水溶液均呈碱性;NaHCO3受热易分解生成Na2CO3、H2O和CO2)。
(1)称取两种固体各1g分别放入两支试管中,在各加入5mL水,振荡。固体成分溶解,并恢复至室温。
①发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,________。
②向所得溶液中各滴入1~2滴酚酞溶液后,溶液均显________色。
(2)①取少量NaHCO3按下图装置进行实验。可观察到的现象是:大试管口有水珠生成,________________。
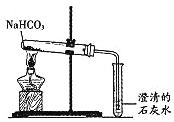
②用______________的方法除去混在Na2CO3粉末中少量的NaHCO3。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_________________;证明反应后氯化钙有剩余的方法是______________________________。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催化剂。以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:
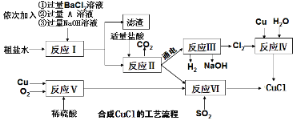
(1)A溶液中溶质的化学式是__________ ;
(2)写出反应V的化学方程式 _______________ ;
(3)反应VI的化学方程式是:2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4,反应中化合价升高的元素是___;
(4)本工艺中可循环利用的物质是NaOH和_____;
(5)反应VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。真空干燥的目的是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性课题小组对氢氧化钠溶液和稀盐酸中和反应的有关问题,进行了如下探究:
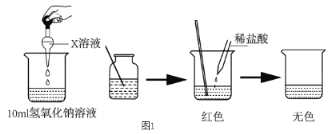
I:(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了图 1所示实验,则 X溶液是_____________。
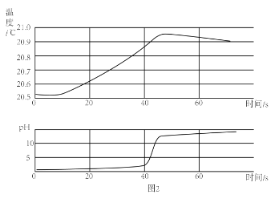
(2)乙同学用传感器探究稀 NaOH 溶液与稀盐酸反应过程中温度和 pH的变化。测定结果如图2所示。通过分析可知,稀 NaOH 溶液与稀盐酸反应会__________(放出”或“吸收”)热量。30s 时,溶液中的溶质为 _____________(写化学式)
II:丙同学为了验证上述实验,也将盐酸滴入某氢氧化钠溶液中,发现有气泡产生,他认为该氢氧化钠溶液已经变质,变质原因用化学方程式可表示为 ____________________。
III:为了测定该氢氧化钠溶液中碳酸钠的质量分数,丙同学设计了如图3所示的实验装置。已知分液漏斗中装有 10%的稀盐酸,装置内试剂均足量。
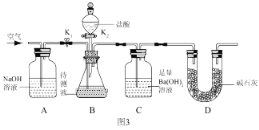
(实验步骤)
①按如图 3 连接好装置后,并检查装置气密性;
②关闭 K1 和 K2,向 B 装置中加入 100.0g该氢氧化钠溶液样品(忽略原装置内空气中CO2对实验的影响);
③打开 K2,向锥形瓶内滴加盐酸,直到 B 中不再产生气泡为止;
④打开 K1 关闭 K2,通入一段时间空气,至装置 C 中不再产生沉淀为止;
⑤将装置 C 中的固液混合物过滤、洗涤、烘干后称得固体质量为 5.0g。
(实验分析及数据处理)
①A 装置的作用是 ____________________。
②若缺少步骤④,则测定结果将 __________(填“偏大”、“偏小”或“不变”)。
③利用实验数据,计算该氢氧化钠溶液中碳酸钠的质量分数为 5.3%。
(实验反思)
下列各项措施中,能提高测定准确度的是 __________(填字母)
A.缓缓滴加稀盐酸
B.在装置 A、B 之间增加盛有浓硫酸的洗气瓶
C.在装置 B、C 之间增加盛有饱和 NaHCO3 的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是新型多功能水处理剂。其生产工艺如下:

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,写出温度较高时反应的离子方程式____________。
(2)在溶液I中加入NaOH固体的目的是_______(填字母)。
A.与反应液I中过量的Cl2继续反应,生成更多的NaClO
B.NaOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使NaClO3转化为NaClO
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图1为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4的生成率的影响。

工业生产中最佳温度为_______,此时Fe(NO3)3与NaClO两种溶液的最佳质量浓度之比为_____。
(4)反应③中的离子反应方程式为_________________;溶液Ⅱ中加入饱和KOH得到湿产品的原因是__________________。
(5)高铁酸钾作为水处理剂是能与水反应其离子反应是:4FeO42-+l0H2O=4Fe(OH)3(胶体)十3O2↑+8OH-。则其作为水处理剂的原理是:①_______________;②_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔导电材料。下列说法一定正确的是( )

A. 该电池工作时,电子的流向外电路由A到B,内电路由B到A形成闭合回路
B. 电极B附近的HNO3浓度增大
C. A电极的反应为:NO2-e-+H2O==NO3-+2H+ NO-3e-+2H2O===NO3-+4H+
D. 该电池工作时,每消耗11.2LO2(标准状况下),可以除去含1molNO和NO2的混合尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用湿法炼锌产生的铜镉渣生产金属镉的流程如下:

已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③______等。已知浸出的金属离子均为二价,写出浸出钴的化学方程式__________________。
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为________________________________。
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为______________________________,
②再加入ZnO控制反应液的pH范围为_____________。
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是______________,若加入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证_________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是____。
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Ksp(CdCO3)=5.210-12, Ksp(CdS)=3.610-29,Ksp(Cd(OH)2)=2.010-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是____________。
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近几年来,冠以“绿色”的新概念不断产生,如绿色食品、绿色材料、绿色能源、绿色化学等,这里的“绿色”是对人类社会可持续发展战略的形象表达。“绿色化学”要求从经济、环保和技术上设计可行的化学反应。据此,由单质镁制硝酸镁的下列四个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
A.Mg![]() Mg(NO3)2
Mg(NO3)2
B.Mg![]() MgCl2
MgCl2![]() Mg(OH)2
Mg(OH)2![]() Mg(NO3)2
Mg(NO3)2
C.Mg![]() MgO
MgO![]() Mg(NO3)2
Mg(NO3)2
D.Mg![]() MgSO4
MgSO4![]() Mg(NO3)2
Mg(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵分解反应为NH2COONH4(s)![]() 2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是
A. 密闭容器中氨气的体积分数不变
B. 1 mol NH2COONH4分解同时有17g NH3消耗
C. 密闭容器中混合气体的密度不变
D. 混合气体的平均分子量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com