
| A. | 0.6mol | B. | 1mol | C. | 1.3mol | D. | 0.8mol |
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时电池内部Li+向正极移动 | |
| B. | 该电池不能选用水做溶剂的电解质 | |
| C. | 充电时,正极的电极反应式:0.45Li++Li0.55CoO2+0.45e-=LiCoO2 | |
| D. | 充电时,外接电源的正极与电池上标注“+”的电极连接 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2O2分解过程中,溶液的pH逐渐下降 | |
| B. | Fe3+是该反应的催化剂 | |
| C. | 2H2O(l)+O2(g)=2H2O2(aq)在一定条件下能够自发进行 | |
| D. | v(H2O2)=2v(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
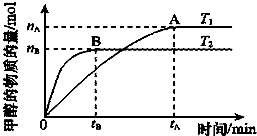 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10% | B. | 50% | C. | 90% | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) | |
| C. | 保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,n(Z)=0.24 mol | |
| D. | 其他条件不变,向平衡体系中再充入0.16 mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaN3是还原剂 | |
| B. | 氧化产物与还原产物物质的量之比为1:15 | |
| C. | N2既是氧化产物又是还原产物 | |
| D. | 标准状况下,当有10mol电子转移时生成358.4L N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25mL | B. | 250mL | C. | 50mL | D. | 500mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com