
【题目】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反 应mX(g) ![]() nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确的是( )
气体体积/L c(Y)/molL-1 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
A.m>n+p
B.Q<0
C.温度不变,压强增大,Y的体积分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室通过如下图所示装置制备Na2S2O3。
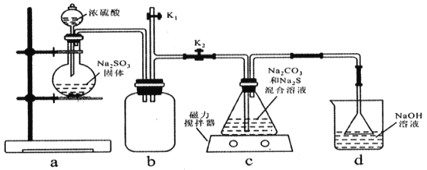
(1)装置a中盛装Na2SO3固体的仪器名称是________。
(2)装置b的作用是_______。
(3)实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有________(填化学式)。
(4)装置c中反应的化学方程式为_____________。
(5)实验结束后,装置c的溶液中溶质主要是Na2S2O3,还含有Na2CO3、Na2SO3等成份。为了证明Na2CO3的存在,设计如下实验。供选试剂:A品红溶液;B酸性高锰酸钾溶液;C BaCl2溶液;D澄清石灰水;E 稀硫酸
① 取C中溶液少许,滴加足量___________(填试剂标号)。
② 将①产生的气体依次通过________(填试剂标号〉,实验现象和结论为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是( )
A. 胆矾、石膏、漂白粉都是纯净物
B. 氢氧化钙、HCl溶液、硫酸铜均为强电解质
C. 氯化钙、烧碱、聚苯乙烯均为化合物
D. 稀豆浆、鸡蛋清溶液、雾均为胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的区别的叙述,正确的是( )
A.胶体带电荷,溶液不带电荷
B.溶液中通过一束光线时没有明显现象,胶体中通过一束光线时出现明显的光路
C.胶体微粒带电荷,溶液中溶质微粒不带电荷
D.在胶体中通电时,分散质微粒向某一极移动,在溶液中通电时,溶质微粒分别向两极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E、F的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E、F均能形成共价化合物。A和B形成的化合物在水中呈碱性。回答下列问题:
(1)五种元素中,原子半径最大的元素在周期表中的位置:__________________,非金属性最强的元素其原子结构示意图为:__________________________;
(2)能说明E、F非金属性强弱的事实是___________________(用一个化学方程式举例);
(3)用电子式表示C、E元素组成的化合物的形成过程:____________________________;
(4)由A和B、D、E、F所形成的共价化合物中,热稳定性最差的是_______(用化学式表示);
(5)D在不充足的F中燃烧,生成的主要产物的结构式为_________________________;
(6)A和F形成的化合物与A和B形成的化合物反应,产物的电子式为_________________,其中存在的化学键类型为___________________________;
(7)写出F的同主族短周期元素的单质与水反应的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A. 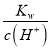 <1.0×10-7mol/L
<1.0×10-7mol/L
B. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分.

(1)写出元素符号: A________、F________。
(2)根据A~H元素在周期表中的位置,选适当的化学式或方程式填入空白处。
①单质中氧化性最强的是________,还原性最强的是________。
②最高价氧化物对应水化物碱性最强的是________,气态氢化物水溶液酸性最强的是_______。
③写出C的单质与B的最高价氧化物水化物溶液反应的离子方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B、C、D四种物质混合放入VL密闭容器中,发生如下反应:aA+bB![]() cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了0.5nmol,C增加了1.5n mol,D增加了n mol。此时反应达到平衡。
cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了0.5nmol,C增加了1.5n mol,D增加了n mol。此时反应达到平衡。
(1)以B的浓度变化表示的该反应的速率为v (B)= 。
(2)该化学方程式中,各物质的化学计量数分别为:a b c d
(3)若只改变压强,反应速率变化但平衡状态不移动,则各物质的聚集状态分别是:A B D 。若在上述平衡混合物中再加入B物质,上述平衡
A.向正反应方向移动 B.向逆反应方向移动
C.不移动 D.条件不够,无法判断
(4)若只升高温度,反应一段时间后,测知四种物质的物质的量又达到相等,则该反应为 反应。(填“放热”或“吸热”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已准确称量过的氯化钠固体配制1.00 mol·L-1的氯化钠溶液0.5 L,要用到的仪器是( )
①500 mL容量瓶 ②试管 ③烧瓶 ④胶头滴管 ⑤烧杯
⑥玻璃棒 ⑦托盘天平 ⑧药匙
A.①④⑤⑥
B.①②④⑤
C.①④⑤⑥⑦⑧
D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com