
 .
.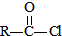
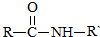 $\stackrel{Na溶液}{→}$RCOONa+R′-NH2
$\stackrel{Na溶液}{→}$RCOONa+R′-NH2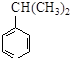 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式 .
.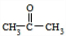 ;扑热息痛的结构简式为
;扑热息痛的结构简式为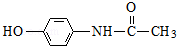 .
. .
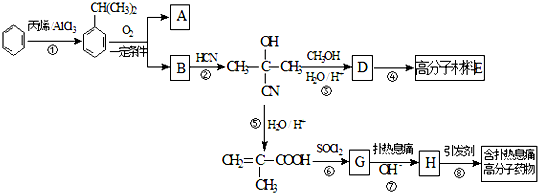
.分析 苯和丙烯在氯化铝存在条件下发生加成反应生成异丙苯,异丙苯被氧化生成A和B,B和氢氰酸发生加成反应生成 ,则B为
,则B为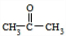 ,1mol
,1mol  可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是 .
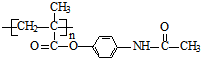
. 与甲醇/水、H+发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是16×6.25=100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=$\frac{60%}{12}$:$\frac{8%}{1}$:$\frac{32%}{16}$=5:8:2,则D的分子式为C5H8O2,D的不饱和度为$\frac{2×5+2-8}{2}$=2,所以D中含有碳碳双键,且含有酯基,则D的结构简式为CH2=C(CH3)COOCH3;D发生加聚反应生成E为
与甲醇/水、H+发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是16×6.25=100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=$\frac{60%}{12}$:$\frac{8%}{1}$:$\frac{32%}{16}$=5:8:2,则D的分子式为C5H8O2,D的不饱和度为$\frac{2×5+2-8}{2}$=2,所以D中含有碳碳双键,且含有酯基,则D的结构简式为CH2=C(CH3)COOCH3;D发生加聚反应生成E为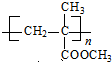 .由反应信息II可知
.由反应信息II可知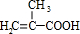 和SOCl2发生取代反应生成G为CH2=C(CH3)COCl,G与扑热息痛反应生成H,H反应生成
和SOCl2发生取代反应生成G为CH2=C(CH3)COCl,G与扑热息痛反应生成H,H反应生成 ,则H为
,则H为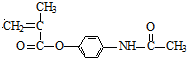 ,扑热息痛的结构简式为
,扑热息痛的结构简式为 ,据此解答.
,据此解答.
解答 解:苯和丙烯在氯化铝存在条件下发生加成反应生成异丙苯,异丙苯被氧化生成A和B,B和氢氰酸发生加成反应生成 ,则B为
,则B为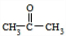 ,1mol
,1mol  可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是 .
. 与甲醇/水、H+发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是16×6.25=100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=$\frac{60%}{12}$:$\frac{8%}{1}$:$\frac{32%}{16}$=5:8:2,则D的分子式为C5H8O2,D的不饱和度为$\frac{2×5+2-8}{2}$=2,所以D中含有碳碳双键,且含有酯基,则D的结构简式为CH2=C(CH3)COOCH3;D发生加聚反应生成E为
与甲醇/水、H+发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是16×6.25=100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=$\frac{60%}{12}$:$\frac{8%}{1}$:$\frac{32%}{16}$=5:8:2,则D的分子式为C5H8O2,D的不饱和度为$\frac{2×5+2-8}{2}$=2,所以D中含有碳碳双键,且含有酯基,则D的结构简式为CH2=C(CH3)COOCH3;D发生加聚反应生成E为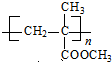 .由反应信息II可知
.由反应信息II可知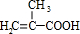 和SOCl2发生取代反应生成G为CH2=C(CH3)COCl,G与扑热息痛反应生成H,H反应生成
和SOCl2发生取代反应生成G为CH2=C(CH3)COCl,G与扑热息痛反应生成H,H反应生成 ,则H为
,则H为 ,扑热息痛的结构简式为
,扑热息痛的结构简式为 .
.
(1)反应①是苯和丙烯发生加成反应,G为CH2=C(CH3)COCl,分子式为 C4H5OCl,
故答案为:加成反应;C4H5OCl;
(2)A是 ,苯酚和过量浓溴水发生取代反应,反应方程式为:
,苯酚和过量浓溴水发生取代反应,反应方程式为: ,
,
故答案为: ;
;
(3)由上述分析可知,B的结构简式为: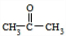 ,扑热息痛的结构简式为:
,扑热息痛的结构简式为: ,
,
故答案为: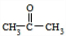 ;
; ;
;
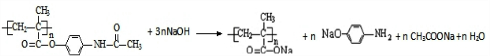
(4)含扑热息痛高分子药物与足量氢氧化钠溶液发生反应的化学方程式为: ,
,
故答案为: ;
;
(5)D为CH2=C(CH3)COOCH3,其同分异构体属于链状酯类,且能发生银镜反应,应为甲酸形成的酯基,则该物质是甲酸某酯,形成酯的醇碳链结构为:C=C-C-C-、C-C=C-C-(有顺反)、C-C-C=C-(有顺反)、C=C(C)-C-、C=C-C(C)-、C-C(C)=C-、C-C=C(C)-(有顺反)、C=C(C-C)-,所以D的符合条件的同分异构体有11种,
故答案为:11.
点评 本题考查有机物的推断与合成,根据转化中有机物的结构、反应条件与给予的信息采用正逆相结合的方法进行分析,熟练掌握官能团的性质与转化,难点是同分异构体种类的判断,注意有碳链异构、官能团异构和顺反异构,难度较大.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:实验题
为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液E,某学生设计如下实验方案:

(1)操作①主要是将固体溶解,则所用的主要玻璃仪器是_____ __、____ ___。
(2)操作②~④加入的试剂依次可以为(写化学式):______________________________;
(3)如何判断SO42-已除尽?_________ ____ ___;
(4)写出加入适量盐酸调PH反应的离子方程式_____________________ ____;
(5)该 同学的实验设计方案是否严密?请说明理由:________________________________。
同学的实验设计方案是否严密?请说明理由:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
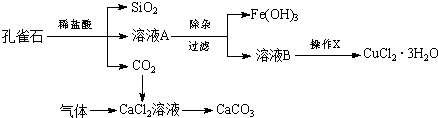
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铁溶于氯化铁溶液:Fe3++Fe═2Fe2+ | |
| C. | 氢氧化钠溶液与硫酸反应:H++OH-═H2O | |
| D. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
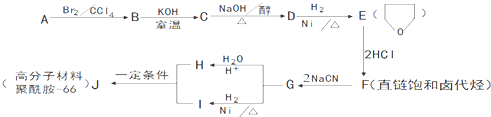
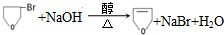 .
. .
. .
.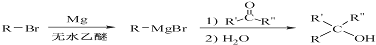
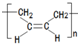
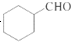 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 阳离子 | H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 | OH-、Cl-、HCO3-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有③④ | C. | 只有②③④ | D. | ①②③④都正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子能透过滤纸,但不能透过半透膜 | |
| B. | Fe(OH)3胶体粒子具有较大的表面积,具有吸附性,能吸附阳离子,故在电场作用下会产生电泳现象 | |
| C. | 向Fe(OH)3胶体中逐滴滴入稀硫酸,会先出现红褐色沉淀然后沉淀消失的现象 | |
| D. | 只有胶体粒子能作布朗运动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com