
| A����ʽ�ζ���δ�ñ�������Һ��ϴ��ֱ��ע���������Һ |
| B���ζ�ǰʢ������������Һ����ƿ������ˮϴ����û�и��� |
| C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ |
| D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ��� |
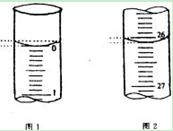
| �ζ����� | ��������������Һ�����/ mL | 0��1000 mol/L ��������/ mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/ mL | ||
| ��һ�� | 25��00 | | | |
| �ڶ��� | 25��00 | 1��56 | 28��08 | 26��52 |
| ������ | 25��00 | 0��22 | 26��34 | 26��12 |
| �ζ����� | ��������������Һ�����/ mL | 0��1000 mol/L ��������/ mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/ mL | ||
| ��һ�� | 25��00 | 0��00 | 26��10 | 26��10 |
| �ڶ��� | 25��00 | 1��56 | 28��08 | 26��52 |
| ������ | 25��00 | 0��22 | 26��34 | 26��12 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��(1) | B��(4) | C��(1)(2) | D��(1)(3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��a>b | B��a=10��4b�� | C��b��10��4a | D��a��b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
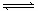 H++OH�� ��H��0������������ȷ���ǣ� ��
H++OH�� ��H��0������������ȷ���ǣ� ��| A����ˮ�м���ϡ��ˮ��ƽ�������ƶ���c(OH��)���� |
| B����ˮ�м������������������ƣ�c(H+)����Kw���� |
| C����ˮ�м�����������NaOH��ƽ�������ƶ���c(OH��)���� |
| D����ˮ���ȣ�Kw����c(H+)���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����֪���������ȶ���С���춡�飬��CH3CH2CH2CH3(g)��(CH3)2CHCH3(g)����H>0 |
B����֪�� OH-(ag)+H+(aq)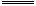 H2O(l)����H="-57.4" kJ/mol H2O(l)����H="-57.4" kJ/mol ��20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ�������� |
C����֪��2H2O(l) 2H2(g)+O2(g)����H=" +483.6" kJ�� mol��1����������ȼ����Ϊ241.8kJ/mol 2H2(g)+O2(g)����H=" +483.6" kJ�� mol��1����������ȼ����Ϊ241.8kJ/mol |
| D����֪��2C(s)+2O2(g)=2CO2(g)����H12C(s)+O2(g)=2CO(g)����H2�����H1>��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��ԭ�����Һ�е�CO2-3��AlO��2�����ʵ���֮��Ϊ1:2 |
| B��V1��V2=l��5 |
| C��M��ʱ���ɵ�CO2Ϊ0.05mol |
| D��a���߱�ʾ�����ӷ���ʽΪ��AlO��2+H++H2O=Al(OH)3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 ________25 �档
________25 �档�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ol/L��Ba��OH��2��Һ����pH��10��Na2S��Һ
ol/L��Ba��OH��2��Һ����pH��10��Na2S��Һ ����pH��5��NH4NO3��Һ�У����������ˮ����
����pH��5��NH4NO3��Һ�У����������ˮ���� �ʵ���֮����( )
�ʵ���֮����( )| A��1:10:1010:109 | B��1:5:5��109:5��108 | C��1:20: 1010:109 | D��1:10:104:109 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com