
| A. | 单质X与A反应的化学方程式:Al2O3+2Fe$\frac{\underline{\;高温\;}}{\;}$Fe2O3+2Al | |
| B. | 检验D溶液中金属阳离子的反应:Fe3++3SCN-=Fe(SCN)3↓ | |
| C. | 单质X和单质Y在一定条件下均能与水发生置换反应 | |
| D. | 由于化合物B和C均既能与酸反应,又能与碱反应,所以两者均是两性氧化物 |
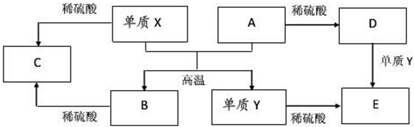
分析 A+X=B+Y是置换反应,单质X、Y都和稀硫酸反应,说明是金属单质,A、B是氧化物和硫酸反应,其中A和硫酸反应生成的D和单质Y反应生成E,说明A中元素化合价是变价,由此可知A和X的置换反应是铝热反应,则X为Al;Y为Fe;A为Fe2O3;B为Al2O3;C为Al2(SO4)3;D为Fe2(SO4)3;E为FeSO4,以此解答该题.
解答 解:A.x与A反应的化学方程式是:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,故A错误;
B.检验D溶液中的金属阳离子为三价铁离子发生反应生成的不是沉淀:Fe3++3SCN-=Fe(SCN)3,故B错误;
C.单质Y为Fe,在高温条件下能与水蒸汽发生置换反应,生成四氧化三铁和氢气,故C正确;
D.由于化合物B为Al2O3既能与酸反应,又能与碱反应,所以是两性化合物,C为Al2(SO4)3是盐不具有两性,故D错误.
故选C.
点评 本题考查了物质转化关系的推断,为高频考点,侧重考查学生的分析能力,注意把握物质性质的应用,反应特征的推断,熟练掌握物质转化关系和特征性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
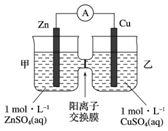
| A. | 锌电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的 c(SO42-)不变 | |
| C. | 电池工作一段时间后,乙池溶液的总质量减少 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ZnMn2O4是负极材料 | |
| B. | 充电时,Zn2+向ZnMn2O4电极迁移 | |
| C. | 充电时,阳极反应:ZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4 | |
| D. | 充放电过程中,只有Zn元素的化合价发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200 mL 2mol/LNaCl溶液 | B. | 75mL 1 mol/L MgCl2溶液 | ||
| C. | 150 mL 3mol/LKCl溶液 | D. | 25 mL 2 mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com