
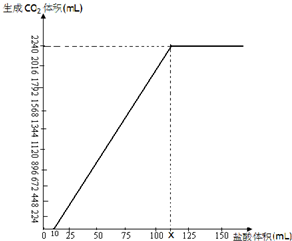
 NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O→Na2CO3•nH2O(n为平均值,n≤10).取没有妥善保管的NaHCO3样品A9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如右图.(已知盐酸滴加至10mL时,开始产生气体,加至15mL时生成CO2112mL,溶解的CO2忽然不计)
NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O→Na2CO3•nH2O(n为平均值,n≤10).取没有妥善保管的NaHCO3样品A9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如右图.(已知盐酸滴加至10mL时,开始产生气体,加至15mL时生成CO2112mL,溶解的CO2忽然不计)分析 (1)溶液中加入盐酸10mL时发生Na2CO3+HCl═NaHCO3+NaCl,加至15mL时生成CO2112mL,发生NaHCO3+HCl═NaCl+CO2↑+H2O,根据二氧化碳来计算稀盐酸的浓度;
(2)由图象可知,将Na2CO3转化为NaHCO3,消耗盐酸10mL,NaHCO3完全反应得到二氧化碳2240mL,根据NaHCO3+HCl═NaCl+CO2↑+H2O计算消耗盐酸的体积,前后两部分盐酸体积之和即为x的值;
(3)由图象可知,溶液中含有碳酸钠,故固体含有Na2CO3?nH2O,将Na2CO3转化为NaHCO3,消耗盐酸10mL,计算转化得到的NaHCO3的物质的量,根据生成的二氧化碳的体积计算溶液中总的NaHCO3物质的量,进而确定原固体中是否含有NaHCO3及其物质的量,再根据固体的质量确定Na2CO3?nH2O中n的值,据此解答
解答 解:(1)溶液中加入盐酸10mL时发生Na2CO3+HCl═NaHCO3+NaCl,加至15mL时生成CO2112mL,发生NaHCO3+HCl═NaCl+CO2↑+H2O,
n(CO2)=$\frac{0.112L}{22.4L/mol}$=0.05mol,则n(HCl)=0.05mol,其浓度为$\frac{0.05mol}{0.05L}$=1mol/L;
答:所加盐酸物质的量浓度为1mol/L;
(2)由图象可知,将Na2CO3转化为NaHCO3,消耗盐酸10mL,NaHCO3完全反应得到二氧化碳2240mL,物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,根据NaHCO3+HCl═NaCl+CO2↑+H2O可知消耗HCl为0.1mol,该阶段消耗盐酸的体积为$\frac{0.1mol}{1mol/L}$=0.1L=100mL,故x=10mL+100mL=110mL,
答:x的值为110;
(3)由图象可知,溶液中含有碳酸钠,故固体含有Na2CO3?nH2O,将Na2CO3转化为NaHCO3,消耗盐酸10mL,由Na2CO3+HCl═NaCl+NaHCO3可知,溶液中n(Na2CO3)=n(HCl)=0.01L×1mol/L=0.01mol,转化生成的NaHCO3的物质的量为0.01mol,由NaHCO3+HCl═NaCl+CO2↑+H2O可知,溶液中总的NaHCO3物质的量为0.1mol,大于0.01mol,故原固体中含有NaHCO3,其物质的量为0.1mol-0.01mol=0.09mol,原固体中Na2CO3?nH2O的质量为9.52g-84g/mol×0.09mol=1.96g,n(Na2CO3?nH2O)=n(Na2CO3),故0.01mol×(106+18n)g/mol=1.96g,解得n=5,故原混合固体含有:NaHCO3为0.09mol、Na2CO3?5H2O为0.01mol,
答:原混合固体含有:0.09molNaHCO3、0.01mol Na2CO3?5H2O.
点评 本题考查混合物的有关计算,题目计算量较大,侧重于月考查学生的分析能力和计算能力,注意利用方程式、极限法与讨论法进行的计算,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、SO42-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| B. | 废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源 | |
| C. | 凡含有食品添加剂的食物对人体健康均有害,不宜食用 | |
| D. | 钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75%的酒精溶液 | B. | 硝酸钠 | C. | Fe(OH)3胶体 | D. | 豆浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com