
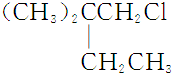 £¬BŗĶD·Ö±šÓėĒæ¼īµÄ“¼ČÜŅŗ¹²ČČ£¬¶¼Ö»ÄܵƵ½ÓŠ»ś»ÆŗĻĪļE£¬ŅŌÉĻ·“Ó¦¼°BµÄ½ųŅ»²½·“Ó¦ČēĻĀĖłŹ¾£¬
£¬BŗĶD·Ö±šÓėĒæ¼īµÄ“¼ČÜŅŗ¹²ČČ£¬¶¼Ö»ÄܵƵ½ÓŠ»ś»ÆŗĻĪļE£¬ŅŌÉĻ·“Ó¦¼°BµÄ½ųŅ»²½·“Ó¦ČēĻĀĖłŹ¾£¬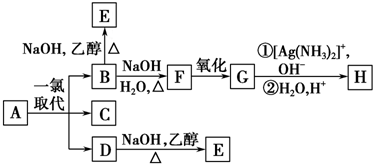
·ÖĪö ĶéĢžAÖ»æÉÄÜÓŠČżÖÖŅ»ĀČČ”“ś²śĪļB”¢CŗĶD£¬CµÄ½į¹¹¼ņŹ½ŹĒ£ØCH3£©2C£ØCH2CH3£©CH2Cl£¬¹ŹAĪŖ£ØCH3£©3CCH2CH3£¬BŗĶD·Ö±šÓėĒæ¼īµÄ“¼ČÜŅŗ¹²ČČ£¬¶¼Ö»ÄܵƵ½ÓŠ»ś»ÆŗĻĪļE£¬¹ŹEĪŖ£ØCH3£©3CCH=CH2£¬BŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗĄļ·¢ÉśĖ®½ā·“Ӧɜ³ÉF£¬FĪŖ“¼£¬FŃõ»ÆÉś³ÉG£¬GÄÜÓėŅų°±ČÜŅŗ·“Ó¦£¬Gŗ¬ÓŠČ©»ł-CHO£¬¹ŹBĪŖ£ØCH3£©3CCH2CH2Cl£¬FĪŖ£ØCH3£©3CCH2CH2OH£¬GĪŖ£ØCH3£©3CCH2CHO£¬HĪŖ£ØCH3£©3CCH2COOH£¬DĪŖ£ØCH3£©3CCH2ClCH3£®
½ā“š ½ā£ŗĶéĢžAÖ»æÉÄÜÓŠČżÖÖŅ»ĀČČ”“ś²śĪļB”¢CŗĶD£¬CµÄ½į¹¹¼ņŹ½ŹĒ£ØCH3£©2C£ØCH2CH3£©CH2Cl£¬¹ŹAĪŖ£ØCH3£©3CCH2CH3£¬BŗĶD·Ö±šÓėĒæ¼īµÄ“¼ČÜŅŗ¹²ČČ£¬¶¼Ö»ÄܵƵ½ÓŠ»ś»ÆŗĻĪļE£¬¹ŹEĪŖ£ØCH3£©3CCH=CH2£¬BŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗĄļ·¢ÉśĖ®½ā·“Ӧɜ³ÉF£¬FĪŖ“¼£¬FŃõ»ÆÉś³ÉG£¬GÄÜÓėŅų°±ČÜŅŗ·“Ó¦£¬Gŗ¬ÓŠČ©»ł-CHO£¬¹ŹBĪŖ£ØCH3£©3CCH2CH2Cl£¬FĪŖ£ØCH3£©3CCH2CH2OH£¬GĪŖ£ØCH3£©3CCH2CHO£¬HĪŖ£ØCH3£©3CCH2COOH£¬DĪŖ£ØCH3£©3CCH2ClCH3£»
£Ø1£©AĪŖ£ØCH3£©3CCH2CH3£¬AµÄĆū³ĘŹĒ2£¬3-¶ž¼×»ł¶”Ķ飬¹Ź“š°øĪŖ£ŗ2£¬3-¶ž¼×»ł¶”Ķ飻
£Ø2£©BĪŖ£ØCH3£©3CCH2CH2Cl£¬FĪŖ£ØCH3£©3CCH2CH2OH£¬B·¢ÉśĖ®½ā·“Ó¦»ņČ”“ś·“Ӧɜ³ÉF£¬·“Ó¦·½³ĢŹ½ĪŖ£ØCH3£©3CCH2CH2Cl+NaOH$”ś_{”÷}^{H_{2}O}$£ØCH3£©3CCH2CH2OH+NaCl£¬
¹Ź“š°øĪŖ£ŗĖ®½ā»ņČ”“ś£»£ØCH3£©3CCH2CH2Cl+NaOH$”ś_{”÷}^{H_{2}O}$£ØCH3£©3CCH2CH2OH+NaCl£»
£Ø3£©EĪŖ£ØCH3£©3CCH=CH2£¬DĪŖ£ØCH3£©3CCH2ClCH3£¬EŗĶNaOHµÄ“¼ČÜŅŗ¼ÓČČ·¢ÉśĻūČ„·“Ӧɜ³ÉE£¬·“Ó¦·½³ĢŹ½ĪŖ£ØCH3£©3CCH2ClCH3+NaOH$”ś_{”÷}^{“¼}$£ØCH3£©3CCH=CH2+NaCl+H2O£¬
¹Ź“š°øĪŖ£ŗ£ØCH3£©3CCH2ClCH3+NaOH$”ś_{”÷}^{“¼}$£ØCH3£©3CCH=CH2+NaCl+H2O£»
£Ø4£©1.16g£ØCH3£©3CCH2COOHµÄĪļÖŹµÄĮæĪŖ$\frac{1.16g}{116g/mol}$=0.01mol£¬ÓÉ£ØCH3£©3CCH2COOH+NaHCO3=£ØCH3£©3CCH2COONa+H2O+CO2”üæÉÖŖ£¬Éś³ÉCO2µÄĪļÖŹµÄĮæĪŖ0.01mol£¬¶žŃõ»ÆĢ¼µÄĢå»żŹĒ0.01mol”Į22.4L/mol=0.224L=224mL£¬¹Ź“š°øĪŖ£ŗ224£»
£Ø5£©CH3£©3CCH2CHOÓėŅų°±ČÜŅŗ·¢ÉśŃõ»Æ·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ
£ØCH3£©3CCH2CHO+2Ag£ØNH3£© 2OH$\stackrel{”÷}{”ś}$£ØCH3£©3CCH2COONH4+2Ag”ż+H2O+3NH3£¬
¹Ź“š°øĪŖ£ŗ£ØCH3£©3CCH2CHO+2Ag£ØNH3£© 2OH$\stackrel{”÷}{”ś}$£ØCH3£©3CCH2COONH4+2Ag”ż+H2O+3NH3£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬ĪŖøßĘµæ¼µć£¬Éę¼°Ķ锢Ā±“śĢž”¢“¼”¢Č©”¢ōČĖįµÄŠŌÖŹÓė×Ŗ»ÆµČ£¬ÄѶČÖŠµČ£¬øł¾ŻAµÄĀ±“ś²śĪļĶʶĻAµÄ½į¹¹ŹĒ¹Ų¼ü£¬Č»ŗóĄūÓĆĖ³ĶĘ·ØĶʶĻ½įŗĻÓŠ»śĪļµÄ·“Ó¦ĢŲµćŗĶŗ¬ÓŠµÄ¹ŁÄÜĶʶĻ£¬ÄѵćŹĒČ©·¢ÉśŅų¾µ·“Ó¦·½³ĢŹ½µÄŹéŠ“£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĪĒåŹÆ»ŅĖ® | B£® | Ę·ŗģČÜŅŗ | C£® | NaOHČÜŅŗ | D£® | ±„ŗĶNaHCO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeCl3 | B£® | Mg3N2 | C£® | SO3 | D£® | Cu2S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ėłŗ¬ÖŹ×ÓŹż=z | B£® | Ėłŗ¬ÖŠ×ÓŹż=A-Z | C£® | Ėłŗ¬µē×ÓŹż=Z+n | D£® | ÖŹĮæŹż=A |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XµÄ×īøßÕż¼Ū±ČYµÄŠ” | |
| B£® | XµÄ×īøß¼ŪŃõ»ÆĪļŅ»¶ØŹĒX2O£¬YµÄĘųĢ¬Ēā»ÆĪļĪŖH2Y | |
| C£® | XµÄĄė×Ó°ė¾¶±ČYµÄ“ó | |
| D£® | XµÄŗĖµēŗÉŹż±ČYµÄŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĀČ»ÆĶ”¢ĀČ»ÆŃĒĶŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬¹ć·ŗÓĆ×÷ÓŠ»śŗĻ³É“߻ƼĮ£®
ĀČ»ÆĶ”¢ĀČ»ÆŃĒĶŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬¹ć·ŗÓĆ×÷ÓŠ»śŗĻ³É“߻ƼĮ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
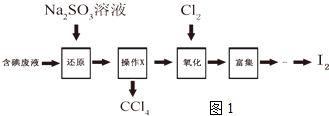
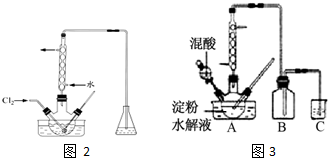
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com