
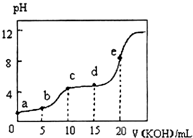
 ³£ĪĀĻĀ£¬ÓĆ0.10mol•L-1KOHČÜŅŗµĪ¶Ø10.00mL 0.10mol•L-1ij¶žŌŖČõĖįH2RČÜŅŗ£¬ĖłµĆµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
³£ĪĀĻĀ£¬ÓĆ0.10mol•L-1KOHČÜŅŗµĪ¶Ø10.00mL 0.10mol•L-1ij¶žŌŖČõĖįH2RČÜŅŗ£¬ĖłµĆµĪ¶ØĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | aµćĖłŹ¾ČÜŅŗÖŠ£ŗ$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$£¼1012 | |
| B£® | cµćĖłŹ¾ČÜŅŗÖŠ£ŗc£ØK+£©£¾c£ØHR-£©£¾c£ØH2R£©£¾c£ØR2-£© | |
| C£® | eµćĖłŹ¾ČÜŅŗÖŠ£ŗc£ØH+£©=c£ØHR-£©+2c£ØH2R£©+c£ØOH-£© | |
| D£® | ĪåøöµćÖŠdµćŹ±c£ØHR-£©×ī“ó |
·ÖĪö A.0.10mol•L-1 H2R£Ø¶žŌŖČõĖį£©²»ÄÜĶźČ«µēĄė£»
B£®cµćČÜÖŹĪŖKHR£¬ČÜŅŗĻŌĖįŠŌ£¬HR-µÄµēĄė³Ģ¶Č“óÓŚĖ®½ā³Ģ¶Č£»
C£®eµćĖłŹ¾ČÜŅŗÖŠČÜÖŹĪŖK2R£¬øł¾ŻÖŹ×ÓŹŲŗć·ÖĪö£»
D£®cµćČÜÖŹĪŖKHR£¬Ōņc£ØHR-£©×ī“ó£®
½ā“š ½ā£ŗA.0.10mol•L-1 H2R£Ø¶žŌŖČõĖį£©²»ÄÜĶźČ«µēĄė£¬c£ØH+£©£¼0.1mol/L£¬Ōņ$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$£¼1012£¬¹ŹAÕżČ·£»
B£®cµćĪŖKHR£¬ČÜŅŗĻŌĖįŠŌ£¬HR-µÄµēĄė³Ģ¶Č“óÓŚĖ®½ā³Ģ¶Č£¬Ōņc£ØK+£©£¾c£ØHR-£©£¾c£ØR2-£©£¾c£ØH2R£©£¬¹ŹB“ķĪó£»
C£®eµćĖłŹ¾ČÜŅŗÖŠČÜÖŹĪŖK2R£¬ČÜŅŗÖŠÖŹ×ÓŹŲŗćĪŖ£ŗc£ØOH-£©=c£ØHR-£©+2c£ØH2R£©+c£ØH+£©£¬¹ŹC“ķĪó£»
D£®cµćČÜÖŹĪŖKHR£¬HR-µÄµēĄė³Ģ¶ČŗĶĖ®½ā³Ģ¶Č¶¼ŗÜŠ”£¬ŌņcµćŹ±c£ØHR-£©×ī“󣬹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĖį¼ī»ģŗĻČÜŅŗµÄ¶ØŠŌÅŠ¶Ļ¼°Ąė×ÓÅØ¶ČµÄ¹ŲĻµ£¬Ć÷Č·µēŗÉŹŲŗć”¢ĪļĮĻŹŲŗć”¢ÖŹ×ÓŹŲŗć¼“æɽā“š£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¶Ō»ł“”ÖŖŹ¶µÄÓ¦ÓĆÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 28gŅŅĻ©ŗĶ»·¶”ĶéµÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ2NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬46gNO2ŗĶN2O4µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ3NA | |
| C£® | ±ź×¼×“æöĻĀ£¬22.4LĖ®ÖŠŗ¬ÓŠµÄÖŹ×ÓŹżĪŖ10NA | |
| D£® | 1molNaÓė×ćĮæµÄO2·“Ó¦£¬Éś³ÉNa2OŗĶNa2O2µÄ»ģŗĻĪļ£¬×ŖŅʵē×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĻņÉĻ·ēæŚ×ŖŅĘ | B£® | ĻņĻĀ·ēæŚ×ŖŅĘ | ||
| C£® | ÓĆŹŖĆ«½ķĪę×”æŚ±Ē | D£® | ¼°Ź±“÷ÉĻÓĆĮņĖįČÜŅŗŹŖČó¹żµÄæŚÕÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
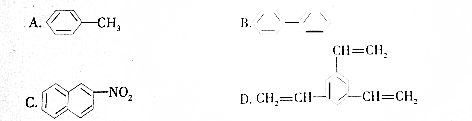
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 µē»ÆѧŌĄķŌŚŅ½Ń§Ņ½ĮĘÖŠÓŠÖŲŅŖÓ¦ÓĆ£®
µē»ÆѧŌĄķŌŚŅ½Ń§Ņ½ĮĘÖŠÓŠÖŲŅŖÓ¦ÓĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com