
【题目】有机物X的结构![]()
![]() 其中Ⅰ、Ⅱ为未知部分的结构
其中Ⅰ、Ⅱ为未知部分的结构![]() 下列是X发生反应的转化关系图及E的信息.
下列是X发生反应的转化关系图及E的信息.
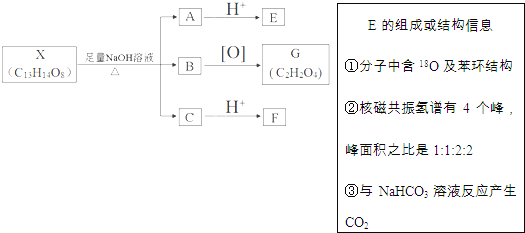
回答下列问题:
![]() 中官能团的名称为 ______ ,F不能发生和化学反应类型有 ______
中官能团的名称为 ______ ,F不能发生和化学反应类型有 ______
A.取代反应 ![]() 加成反应
加成反应 ![]() 氧化反应
氧化反应 ![]() 消去反应
消去反应
![]() 的分子式为 ______ B与G反应可生成高分子化合物M,其化学方程式是 ______
的分子式为 ______ B与G反应可生成高分子化合物M,其化学方程式是 ______
![]() 在足量NaOH溶液中反应的化学方程式为 ______
在足量NaOH溶液中反应的化学方程式为 ______
![]() 化合物E有多种同分异构体,满足下列条件的所有同分异构体有 ______ 种,任写其中一种的结构简式为 ______
化合物E有多种同分异构体,满足下列条件的所有同分异构体有 ______ 种,任写其中一种的结构简式为 ______
![]() 遇氯化铁溶液显紫色;
遇氯化铁溶液显紫色;![]() 分子中除苯环外物其中它环;
分子中除苯环外物其中它环;![]() 能发生眼镜反应.
能发生眼镜反应.
【答案】羧基、羟基 B ![]() nHOOC-COOH+nHOCH2CH2OH
nHOOC-COOH+nHOCH2CH2OH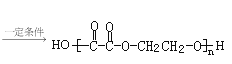 +(2n-1)H2O
+(2n-1)H2O ![]() +4NaOH
+4NaOH![]()
![]()
![]() 9
9 ![]()
【解析】
有机物X的分子式为C13H14O8,在碱性条件下水解得到A、B、C,可推知X中含有酯基,A与酸反应得到E,E能与碳酸氢钠反应生成二氧化碳,则E含有-COOH,E中有18O及苯环结构,结合X的结构片段、B氧化生成G的分子式C2H2O4,可知A中含有7个碳原子,则F的结构简式为HOOCCH2CH(OH)COOH,逆推可知C为NaOOCCH2CH(OH)COOONa,E中有苯环且有4种氢,其个数比为1:1:2:2,可推知E为![]() ,A为
,A为![]() ,结合X的结构片段可知B为HOCH2CH2OH,G的分子式为C2H2O4,且是B的氧化产物,所以G为HOOC-COOH,综上分析可知X为
,结合X的结构片段可知B为HOCH2CH2OH,G的分子式为C2H2O4,且是B的氧化产物,所以G为HOOC-COOH,综上分析可知X为![]() ,据此分析解答。
,据此分析解答。
(1)F的结构简式为![]() ,含有官能团有:羧基、羟基,可以发生取代反应、氧化反应、消去反应,不能发生加成反应,故答案为:羧基、羟基;B;
,含有官能团有:羧基、羟基,可以发生取代反应、氧化反应、消去反应,不能发生加成反应,故答案为:羧基、羟基;B;
(2)B为![]() ,分子式为
,分子式为![]() ,B与G反应可生成高分子化合物M为
,B与G反应可生成高分子化合物M为![]() ,该反应方程式为:n HOOC-COOH+n HOCH2CH2OH
,该反应方程式为:n HOOC-COOH+n HOCH2CH2OH![]()
![]() +(2n-1)H2O, 故答案为:
+(2n-1)H2O, 故答案为:![]() ;n HOOC-COOH+n HOCH2CH2OH
;n HOOC-COOH+n HOCH2CH2OH![]()
![]() +(2n-1)H2O;
+(2n-1)H2O;
(3)X在足量NaOH溶液中反应的化学方程式为:![]() +4NaOH
+4NaOH ![]()
![]() +NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O, 故答案为:
+NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O, 故答案为:![]() +4NaOH
+4NaOH ![]()
![]() +NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O;
+NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O;
(4)化合物![]()
![]()
![]() 有多种同分异构体,①遇氯化铁溶液显紫色,含有酚羟基;②分子中除苯环外物其中它环;③能发生眼镜反应,含有醛基,含有2个侧链为
有多种同分异构体,①遇氯化铁溶液显紫色,含有酚羟基;②分子中除苯环外物其中它环;③能发生眼镜反应,含有醛基,含有2个侧链为![]() 、
、![]() ,有邻、间、对三种位置,可以含有2个
,有邻、间、对三种位置,可以含有2个![]() 、1个
、1个![]() ,若2个
,若2个![]() 处于邻位,
处于邻位,![]() 有2种位置,若2个
有2种位置,若2个![]() 处于间位,
处于间位,![]() 有3种位置,若2个
有3种位置,若2个![]() 处于对位、
处于对位、![]() 有1种位置,符合条件的同分异构体共有
有1种位置,符合条件的同分异构体共有![]() 种,其中一种同分异构体为
种,其中一种同分异构体为![]() 等,故答案为:9;
等,故答案为:9;![]() 等。
等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】白藜芦醇广泛存在于食物(例如桑甚、花生,尤其是葡萄)中,它可能具有抗癌性。能够与1 mol该化合物发生反应的Br2和H2的最大用量分别是( )
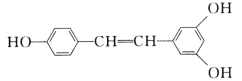
A.1mol、1molB.3.5mol、7mol
C.3.5mol、6molD.6mol、7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气(CO和H2)是目前化工常用的原料,下面是用甲烷制备合成气的两种方法:
① CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;
② 2CH4(g)+O2(g) ![]() 2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。
2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。
其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是( )

A. E1表示2CH4(g)+O2(g) ![]() 2CO(g)+4H2(g)的活化能
2CO(g)+4H2(g)的活化能
B. E2表示CH4(g)+H2O(g)![]() CO(g)+3H2(g)的活化能
CO(g)+3H2(g)的活化能
C. 该图示为反应②的反应过程与能量变化示意图
D. 一般情况下,加入催化剂,既能降低E1,也能降低E2,但不能改变E1与E2的差值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的自动化检测中常常应用根据原电池原理设计的传感器。下图为电池的工作示意图,气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。
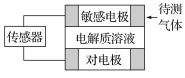
待测气体 | 部分电极反应产物 |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |
则下列说法中正确的是
A. 上述气体检测时,敏感电极均作电池负极
B. 检测Cl2气体时,敏感电极的电极反应式为Cl2+2e-===2Cl-
C. 检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+2H2O+4e-===4OH-
D. 检测Cl2和CO体积分数相同的两份空气样本时,传感器上电流大小、方向相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为____。
(2)反应前A的物质的量浓度是____。
(3)10 s末,生成物D的浓度为__。
(4)A与B的平衡转化率之比为___。
(5)反应过程中容器内气体的平均相对分子质量变化是_(填“增大”、“减小”或“不变”,下同),气体的密度变化是___。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____;②增大A的浓度_____;
③恒容下充入氖气________。
(7)下列叙述能说明该反应已达到化学平衡状态的是(填标号)___;
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
(8)将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) ![]() NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g) ![]() H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为___。
H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白雾产生,是因为生成了___________气体,发生的反应方程式______________________________。采用分液漏斗滴加溴的方式,这样的好处是_______________;c的作用_________________; 冷凝水的方向是________________(填写“上进下出”或者“下进上出”);
(2)液溴滴完后,经过下列步骤分离提纯:
(a)向a中加入10mL水,然后通过过滤除去未反应的铁屑;
(b)滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是_________;
(c)向分出的粗溴苯中加入少量的无水硫酸镁,静置、过滤。加入硫酸镁的目的是_____;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须的是________(填入正确选项前的字母);
a.重结晶 b.过滤 c.蒸馏 d.萃取
(4)在该实验中,a的容积最适合的是___(填入正确选项前的字母)。
a.25mL b.50mL c.250mL d.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH和体积均相同的HNO2和CH3COOH溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
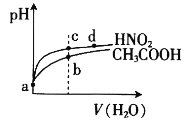
A.电离平衡常数:Ka(CH3COOH)>Ka(HNO2)
B.从c点到d点,溶液中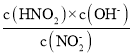 的值保持不变
的值保持不变
C.溶液中水的电离程度:b>c
D.a点时,相同体积的两溶液分别与NaOH恰好中和后,溶液中的n(Na+)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学仿照“喷泉”实验的原理,在实验室中做了一个“喷烟”实验,如图所示。他在甲、乙两个烧瓶中分别充入X、Y两种无色气体,在胶头滴管中盛有含酚酞的NaOH溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可以看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。若已知X、Y是HCl、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、NO其中气体中的两种,则下列判断中,正确的是( )
、NO其中气体中的两种,则下列判断中,正确的是( )

A.X是![]() ,Y是HClB.X是
,Y是HClB.X是![]() ,Y是
,Y是![]()
C.X是![]() ,Y是
,Y是![]() D.X是NO,Y是
D.X是NO,Y是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com