
ĖÄÖÖÖ÷×åŌŖĖŲµÄĄė×Óa Xm+£¬bYn+£¬cZn-ŗĶdRm-£Øa£¬b£¬c£¬dĪŖŌŖĖŲµÄŌ×ÓŠņŹż£©£¬ĖüĆĒ¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬Čōm£¾n£¬¶ŌĻĀĮŠŠšŹöµÄÅŠ¶ĻÕżČ·µÄŹĒ(””””)
¢Ła£b£½n£m ¢ŚŌŖĖŲµÄŌ×ÓŠņŹża£¾b£¾c£¾d
¢ŪŌŖĖŲ·Ē½šŹōŠŌZ£¾R ¢Ü×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ¼īŠŌX£¾Y
| A£®¢Ś¢ŪÕżČ· | B£®Ö»ÓŠ¢ŪÕżČ· | C£®¢Ł¢Ś¢Ū¢ÜÕżČ· | D£®¢Ł¢Ś¢ŪÕżČ· |
A
½āĪöŹŌĢā·ÖĪö£ŗa Xm+ÖŠaĪŖÖŹ×ÓŹż”£¶ųµē×ÓŹżĪŖa-m.,¶ų bYn+µÄµē×ÓŹżĪŖb-n
cZnµÄµē×ÓŹżĪŖc+n dRm-µÄµē×ÓŹżĪŖd+m.ÓÉÓŚĖüĆĒ¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹ĖłŅŌa-m.,=
b-n¹Ź¢ŁŹĒ“ķĪóµÄ”£¶ų¢ÜÖŠ£¬XÓėYÓ¦ŹōÓŚĶ¬Ņ»øöÖÜĘŚ£¬ĒŅm£¾nĖłŅŌXµÄŌ×ÓŠņŹżÓ¦øƱČY µÄŅŖ“ó£¬ĖłŅŌXµÄ°ė¾¶±ČYµÄŅŖŠ”£¬°ė¾¶Ō½Š”£¬¼īŠŌŌ½Čõ£¬ĖłŅŌ¼īŠŌÓ¦øĆŹĒYµÄĒ攣¹Ź¢ÜŹĒ“ķĪóµÄ”£ĖłŅŌ“š°øŃ”A
æ¼µć£ŗæ¼²éĄė×Óµē×ÓŹżµÄ¼ĘĖćŅŌ¼°ŌŖĖŲÖÜĘŚĀɵÄĻą¹ŲÖŖŹ¶µć


 ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø
ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø ³å“Ģ100·Öµ„ŌŖÓÅ»ÆĮ·æ¼¾ķĻµĮŠ“š°ø
³å“Ģ100·Öµ„ŌŖÓÅ»ÆĮ·æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ½įĀŪ“ķĪóµÄŹĒ
| A£®Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗHF>HCl>H2S>PH3£¾SiH4 | B£®Ī¢Į£°ė¾¶£ŗK+£¾Al3+£¾S2-£¾Cl”Ŗ |
| C£®ĖįŠŌ£ŗH2SO4£¾CH3COOH£¾H2CO3£¾HClO | D£®½šŹōŠŌ£ŗK>Ca>Mg>Be |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ1”«18ŗÅŌŖĖŲµÄĄė×ÓaW3+”¢bX+”¢cY2-”¢dZ - ¶¼¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬ĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ£Ø £©
| A£®Ąė×ӵĻ¹ŌŠŌ£ŗY2-£¾Z- | B£®ÖŹ×ÓŹż£ŗc£¾b |
| C£®Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗH2Y£¾HZ | D£®Ō×Ó°ė¾¶£ŗX£¼W |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ±Č½Ļ»ņ¹éÄÉÕżČ·µÄŹĒ( )
| A£®ĪČ¶ØŠŌ£ŗNH3<PH3<ASH3 |
| B£®Ąė×Ó°ė¾¶£ŗCl->S2->Al3+ |
| C£®ĖįŠŌ£ŗHClO4>H2SO4>H3PO4 |
| D£®¼īŠŌ£ŗBe£ØOH£©2>Mg£ØOH£©2>Al£ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĖµ·Ø²»·ūŗĻ¢÷A×åŌŖĖŲŠŌÖŹĢŲÕ÷µÄŹĒ
| A£®Ņ׊Ī³É£1¼ŪĄė×Ó | B£®“ÓÉĻµ½ĻĀŌ×Ó°ė¾¶Öš½„¼õŠ” |
| C£®“ÓÉĻµ½ĻĀ·Ē½šŹōŠŌÖš½„¼õČõ | D£®“ÓÉĻµ½ĻĀĒā»ÆĪļµÄĪČ¶ØŠŌŅĄ“Ī¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠŌŖĖŲÖŠ»łĢ¬Ō×ӵĵŚŅ»µēĄėÄÜ×ī“óµÄŹĒ( )
| A£®B | B£®C | C£®N | D£®O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠÓŠ¹ŲŌ×Ó½į¹¹ŗĶŌŖĖŲÖÜĘŚĀɵıķŹöÕżČ·µÄŹĒ £Ø £©
¢ŁŌ×ÓŠņŹżĪŖ15µÄŌŖĖŲµÄ×īøß»ÆŗĻ¼ŪĪŖ+3 ¢Ś¢÷A×åŌŖĖŲŹĒĶ¬ÖÜĘŚÖŠ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲ ¢ŪµŚ¶žÖÜĘŚ¢ōA×åŌŖĖŲµÄŌ×ÓŗĖµēŗÉŹżŗĶÖŠ×ÓŹżŅ»¶ØĪŖ6 ¢ÜŌ×ÓŠņŹżĪŖ12µÄŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚČżÖÜĘŚ¢ņA×å
| A£®¢Ł¢Ś | B£®¢Ł¢Ū | C£®¢Ś¢Ü | D£®¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŌĻĀ±ķŹö²»·ūŗĻŌŖĖŲÖÜĘŚĀɵďĒ
| A£®ĖįŠŌ£ŗH3PO4£¾HNO3£¾HClO4 |
| B£®ČČĪČ¶ØŠŌ£ŗHF£¾H2O£¾NH3 |
| C£®Ąė×Ó°ė¾¶£ŗF££¾Na£«£¾Mg2£« |
| D£®»¹ŌŠŌ£ŗHI£¾HBr£¾HCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
W”¢X”¢Y”¢ZŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹż±ä»ÆČēĻĀĶ¼”£ŅŃÖŖWµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£»XŗĶNeŌ×ÓµÄŗĖĶāµē×ÓŹżĻą²ī1£»YµÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£»ZµÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īĒ攣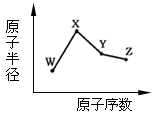
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®¶ŌÓ¦¼ņµ„Ąė×Ó°ė¾¶£ŗZ£¾X£¾W |
| B£®¶ŌÓ¦ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌY£¾Z |
| C£®»ÆŗĻĪļXZW¼Čŗ¬Ąė×Ó¼ü£¬ÓÖŗ¬¹²¼Ū¼ü |
| D£®YµÄŃõ»ÆĪļ¼ČÄÜÓėZµÄĒā»ÆĪļČÜŅŗ·“Ó¦£¬ÓÖÄÜÓėXµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄČÜŅŗ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com