

| A���ܷ���������ԭ��Ӧ��ֻ�Т١��ڡ��ܡ��� |
| B������Ӧ�ٺͷ�Ӧ�۲����������ϣ�������ɫ�����仯 |
| C����Ӧ�����ɵĹ����ڿ����и�������ֻ�����ֽⷴӦ |
| D��������1������3�����ٻ�ϣ��ܼ����������Һ�����ʵ���Ũ�� |
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
10 �� |
| Ũ���ᣬ�� |
| ��Al2O4���� |
8 �� |
| Br2 |
| ��ҺCCl4 |
8 �� |
| A��CH3CH2CHBrCH2Br |
| B��CH3CH��CH2Br��2 |
| C��CH3CHBrCHBrCH3 |
| D����CH3��2CBrCH2Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe3+��NO3-��Cl-��Na+ |
| B��Ca2+��HCO3-��Cl-��K+ |
| C��NH4+��Fe2+��SO42-��NO3- |
| D��Cl-��SO42-��K+��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ���� kJ?mol-1��ʾ��������۲���ͼ��Ȼ��ش����⣮
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ���� kJ?mol-1��ʾ��������۲���ͼ��Ȼ��ش����⣮ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3.01��1023 |
| B��4.816��1023 |
| C��6.02��1023 |
| D��1.204��1024 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
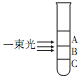 �Ȼ��������еķ�ɢ������ʵ������һ�����ɺܶࡰAgCl����϶��ɵļ����壮��ʢ��NaCl��Һ���Թ��еμ�AgNO3��Һ�����ú���һ���������Թܣ������Թܵ�������ͬ������ֻ��һ������������ԵĶ����ЧӦ�������з�����ȷ���ǣ�������
�Ȼ��������еķ�ɢ������ʵ������һ�����ɺܶࡰAgCl����϶��ɵļ����壮��ʢ��NaCl��Һ���Թ��еμ�AgNO3��Һ�����ú���һ���������Թܣ������Թܵ�������ͬ������ֻ��һ������������ԵĶ����ЧӦ�������з�����ȷ���ǣ�������| A����������A����������AgCl��ֱ����С |
| B����������B����������AgCl��ֱ������A��C����֮�� |
| C����������C����������AgCl��ֱ����� |
| D��������AgCl�Ĵ�С����ͬ����ֻ��B�����з�ɢ�ʵĴ�С����1��100 nm֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�16 g CH4�к��е�ԭ������Ϊ5NA |
| B����״���£�11.2 LCH3OH�к��еĹ��ۼ���ĿΪ2.5NA |
| C�����³�ѹ�£�2.24 L CO��CO2��������к��е�̼ԭ����ĿΪ0.1NA |
| D����״���£�0.1 mol Cl2������������Һ��ȫ���գ�ת�Ƶĵ�����ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
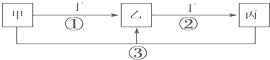 ��֪�ס��ҡ�����������ѧ��ѧ�ij������ʣ��Ҽס��ҡ���������ͬһ��Ԫ�أ���һ������������֮����ת����ϵ��ͼ��ʾ�����ַ�Ӧ�е�H2O����ȥ����
��֪�ס��ҡ�����������ѧ��ѧ�ij������ʣ��Ҽס��ҡ���������ͬһ��Ԫ�أ���һ������������֮����ת����ϵ��ͼ��ʾ�����ַ�Ӧ�е�H2O����ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol�������������22.4 L |
| B��2 mol�Ȼ��ƹ����ܽ���1 Lˮ�����������ʵ���Ϊ2 mol/L |
| C������NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11.2 L |
| D��32 g O2�к�����ԭ����Ϊ1.204��1024 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com