
| A. | 配离子只能存在于晶体中 | |
| B. | 配位体只能是多原子分子 | |
| C. | 配合物的稳定性是指配合物在受热情况下是否易分解 | |
| D. | 血红素中的Fe2+与CO形成的配合物比与O2形成的配合物稳定 |
分析 A.配离子也能存在于溶液中;
B.能作为配合物配位体的微粒需含有孤对电子可以是多原子分子,也可为离子;
C.配合物的稳定性指中心离子和配体的结合能力,配合物中配位键越强,配合物越稳定;
D.配合物中配位键越强,配合物越稳定,中心离子相同,稳定性与配体有关;
解答 解:A.提供空轨道的离子和提供孤电子对的分子或离子能形成配位键,配离子可存在于晶体中,也可存在于溶液中,如:SCN-的电子式 ,铁离子提供空轨道,硫原子提供孤电子对,溶液中络合物Fe(SCN)3含有配位键,故A错误;
,铁离子提供空轨道,硫原子提供孤电子对,溶液中络合物Fe(SCN)3含有配位键,故A错误;
B.能作为配合物配位体的微粒需含有孤对电子,可以是多原子、分子如:NH3是共价化合物,氮原子分别与3个氢原子通过一对共用电子对结合,NH3电子式为 ,有孤对电子,可以作为配体,也可为离子如:Cl-为氯原子得到1个电子形成的阴离子,电子式为
,有孤对电子,可以作为配体,也可为离子如:Cl-为氯原子得到1个电子形成的阴离子,电子式为 ,有孤对电子,可以作为配体,故B错误;
,有孤对电子,可以作为配体,故B错误;
C.配合物的稳定性与配位键强弱有关,键强弱中心离子受电荷、离子半径等影响,配体受酸碱性等影响,所以配合物配位键越强,配合物越稳定,与受热情况下是否易分解无关,故C错误;
D.血红素中的Fe2+分别与CO、O2形成的配合物,中心离子Fe2+相同,配体CO形成的配位键强,所以Fe2+与CO形成的配合物比与O2形成的配合物稳定,所以人体CO易中毒,故D正确;故选D.
点评 本题考查了配合物的有关知识,掌握配合物的构成以及中心离子和配体间的关系是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 10℃20mL3 mol•L-1的X溶液 | B. | 20℃30 mL 2 mol•L-1的X溶液 | ||
| C. | 20℃10 mL 4 mol•L-1的X溶液 | D. | 10℃10 mL 2 mol•L-1的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①②⑤ | C. | ②③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
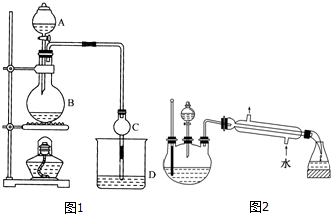
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
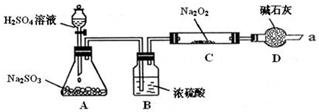

| 实验步骤 | 现象 |
| ①取少量C中固体产物于试管中,加入适量的蒸馏水溶解. | 固体全部溶解 |
| ②向上试管中加入过量的稀盐酸,将产生的气体通入少量酸性KMnO4溶液中. | KMnO4溶液紫色褪去 |
| ③向步骤②反应后的试管中,加入适量的BaCl2溶液. | 产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.002mol(L•s) | B. | v(H2O)=0.002mol/(L•s) | ||
| C. | v(NO)=0.0015mol/(L•s) | D. | v(O2)=0.00125mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2L0.5mol/L亚硫酸溶液中含有的H+个数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com