
最近研制出一种新材料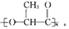 它能代替聚苯乙烯。它是由乳酸(一种有机酸)缩聚而成,能在乳酸菌的作用下降解而不会污染环境。下列关于聚乳酸的说法正确的是
它能代替聚苯乙烯。它是由乳酸(一种有机酸)缩聚而成,能在乳酸菌的作用下降解而不会污染环境。下列关于聚乳酸的说法正确的是
A.聚乳酸是一种纯净物 B.聚乳酸的单体是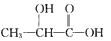
C.聚乳酸是一种羧酸 D.聚乳酸是由其单体通过加聚反应合成的
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
根据实验室中测定硫酸铜晶体(CuSO4·xH2O)结晶水含量的实验,填写下列空白:⑴ 从下列仪器中选出所需仪器(用标号字母填写)_____________________。
A.电子天平 B.试管夹 C.烧杯
D.蒸发皿 E.坩埚 F.石棉网
除上述仪器和酒精灯外,还需要的仪器是____________,________________(任意填写两种)。
⑵ 某学生实验后得到以下数据:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.400 g | 7.900 g | 7.100 g |
①根据以上数据计算该硫酸铜晶体中结晶水x的值为_____________(精确到0.1)。
②若另一学生经实验测得x= 4.9,该学生实验结果产生误差的原因可能是(填写字母)________。
A.没有进行恒重操作 B.加热后在干燥器中冷却至室温后称量
C.加热固体到白色后,露置在空气中冷却 D.加热过程中晶体有少量溅失
查看答案和解析>>
科目:高中化学 来源: 题型:
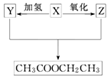
有机物X,经过下列化学变化后可一定条件下得到
乙酸乙酯(如右图),则有机物X是( )
A、C2H5OH B、C2H4
C、CH3CHO D、CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
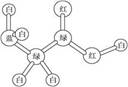
某期刊封面上有如图所示的一个分子的球棍模型。
图中“棍”在表单键或双键或叁键。
不同颜色的球代表不同元素的原子。该模型可代表一种( )
A.卤代羧酸 B.酯 C.氨基酸 D.醇
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某有机物的结构简式为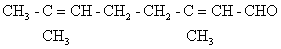
试回答:
(1)检验分子中含有醛基的方法是_____反应,化学方程式为 。
(2)实验操作中,以上哪个官能团应该先检验:_____________________ _ _____。
(3)检验分子中含有碳碳双键的操作是 。
写出上述操作中发生的反应方程式 。
(4)该有机物可以发生下列反应:____________。(填序号)
A.可以和硝酸在一定条件下酯化 B.可以使酸性高锰酸钾褪色
C.可以和溴水发生取代反应 D.可发生加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
以下物质的工业制备原理错误的是 ( )。
A.无水氯化镁的制备:MgCl2·6H2O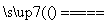 MgCl2+6H2O
MgCl2+6H2O
B.铝的制备:2Al2O3(熔融)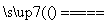 4Al+3O2↑
4Al+3O2↑
C.烧碱的制备:2NaCl+2H2O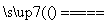 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
D.漂白粉的制备:2Ca(OH)2+2Cl2===Ca(ClO)2+CaCl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)有关研究表明CO2在大气中含量增大,导致地球表面的温度升高,即温室效应。为了控制温室效应,各国科学家提出了不少方法和设想。有人设想将CO2分子液化或制成干冰,封存于地下或海底,以减小大气中CO2的浓度。为使CO2液化,可采用的措施是________。
A.减压、升温  B.增压、升温
B.增压、升温
C.减压、降温 D.增压、降温
快速、有效地减缓大气中的CO2,可采用的生态学措施是____________。
A.使用天然气等燃料 B.控制全球人口增长
C.植树造林,保护森林 D.立即停止煤和石油的燃烧
(2)将一定体积的CO2通入到一定浓度的NaOH溶液中,为了测定其溶液的成分,向该溶液中逐滴加入1 mol·L-1的盐酸。所加入盐酸的体积与产生CO2气体的体积(标准状况)的关系如图所示。
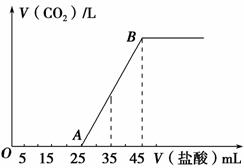

①写出OA段所发生反应的离子方程式_____________________________。
②当加入35 mL盐酸时,产生CO2的体积为____________mL(标准状况)。
③溶液中所含的物质有_______________________,其物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以Ni(NO3)2·6H2O和尿素[CO(NH2)2]为原料制备。
(1)Ni2+的基态核外电子排布式为 。
(2)与NO3-离子互为等电子体的一种分子的分子式为 ,该分子的空间几何构型为 。
(3)尿素分子中碳原子的杂化方式为 ,1mol尿素分子中含有的σ键数为 。
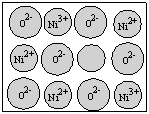 (4)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+-所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6∶91。若该晶体的化学式为NiXO,则X= 。
(4)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+-所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6∶91。若该晶体的化学式为NiXO,则X= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com