
|
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)
| |
| [ ] | |
A. |
温度:T1>T2>T3 |
B. |
正反应速率:v(a)>v(c) v(b)>v(d) |
C. |
平衡常数:K(a)>K(c) K(b)=K(d) |
D. |
平均摩尔质量:M(a)<M(c) M(b)>M(d) |
科目:高中化学 来源: 题型:
(14分)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
已知:① CH4 (g) + H2O (g) = CO(g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+![]() O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③ CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3=+165.0 kJ·mol-1
(1)CH4(g)与CO2 (g)反应生成CO(g)和H2(g)的热化学方程式为 。
(2)从原料选择和能源利用角度,比较方法①和②,为合成甲醇,用甲烷制合成气的适宜方法为 (填序号),其原因是 。
(3)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac + CO + NH3 [Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是 。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。
① O<V≤44.8 L时,电池总反应方程式为 ;
② 44.8 L<V≤89.6 L时,负极电极反应为 ;
③V=67.2 L时,溶液中离子浓度大小关系为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是一种优质的液体燃料,CO和CO2均可用于合成甲醇。
目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) =CH3OH(g)+H2O(g) △H1
(1)已知: 2CO(g) +O2(g) =2CO2(g) △H2
2H2(g)+O2(g) =2H2O(g) △H3
则 CO(g) + 2H2(g) CH3OH(g) 的 △H= 。
(2)由CO合成甲醇时,CO在不同温度下的平衡转化率与压强的关系如下图所示。

该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)一定温度下,向2L密闭容器中加入1mol CH3OH (g),
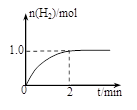
发生反应:CH3OH(g) CO(g) + 2H2(g),H2物质的量随
时间的变化如右图所示。
0~2 min内的平均反应速率v(CH3OH)= 。
该温度下,CO(g) + 2H2(g) CH3OH(g)的平衡常数
K= 。
相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.CH3OH的平衡浓度 c.达到平衡的时间 d.平衡时气体的密度
(4)以CH3OH为燃料(以KOH溶液作电解质溶液)可制成CH3OH燃料电池。
①充入CH3OH的电极为 极;
②负极反应的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省五校协作体高三(高二期末)摸底考试化学试卷(解析版) 题型:填空题
甲醇是一种常用的燃料,工业上可以用CO和H2在一定条件下合成甲醇。
(1)已知CO(g)、H2(g)、CH3OH(1)的燃烧热△H分别为:-283.0kJ/mol、-285.8 kJ/mol、-726.5kJ/mol,则CO合成甲醇的热化学方程式为: 。
(2)在恒容密闭容器中CO与H2发生反应生成甲醇,各物质浓度在不同条件下的变化状况如图所示(开始时氢气的浓度曲线和8分钟后甲醇的浓度曲线未画出。4分钟和8分钟改变的条件不同):

①下列说法正确的是
A.起始时n(H2)为1.7mol
B.当容器内压强恒定时,说明反应达到平衡状态
C.4分钟时,改变的条件是升高温度
D.7分钟时,v(CO)=v(CH3OH)
②计算0~2min内平均反应速率v(H2)=
③在3min时该反应的平衡常数K= (计算结果)
④在图中画出8~12min之间c(CH3OH)曲线
(2)2009年,中国在甲醇燃料电池技术上获得突破,组装了自呼吸电池及主动式电堆,其装置原理如图甲。

①该电池的负极反应式为: 。
②乙池是一铝制品表面“钝化”装置,两极分别为铝制品和石墨。
M电极的材料是 ,该铝制品表面“钝化”时的反应式为: 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三4月双周练习化学试卷(解析版) 题型:填空题
(14分)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
已知:① CH4 (g) + H2O (g) = CO (g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+ O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③ CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3=+165.0 kJ·mol-1
(1)CH4(g)与CO2 (g)反应生成CO(g)和H2(g)的热化学方程式为 。
(2)从原料选择和能源利用角度,比较方法①和②,为合成甲醇,用甲烷制合成气的适宜方法为 (填序号),其原因是 。
(3)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac + CO + NH3  [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是 。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。

① O<V≤44.8 L时,电池总反应方程式为 ;
② 44.8 L<V≤89.6 L时,负极电极反应为 ;
③ V=67.2 L时,溶液中离子浓度大小关系为 。
查看答案和解析>>
科目:高中化学 来源:2013届吉林省高二上学期质量检测化学试卷 题型:填空题
甲醇是一种优质的液体燃料,CO和CO2均可用于合成甲醇。
目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g) +3H2(g) =CH3OH(g)+H2O(g) △H1
(1)已知: 2CO(g) +O2(g) =2CO2(g) △H2
2H2(g)+O2(g) =2H2O(g) △H3
则 CO(g) + 2H2(g)  CH3OH(g) 的 △H=
。
CH3OH(g) 的 △H=
。
(2)由CO合成甲醇时,CO在不同温度下的平衡转化率与压强的关系如下图所示。

该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)一定温度下,向2L密闭容器中加入1mol CH3OH (g),

发生反应:CH3OH(g)
 CO(g) + 2H2(g),H2物质的量随
CO(g) + 2H2(g),H2物质的量随
时间的变化如右图所示。
0~2 min内的平均反应速率v(CH3OH)= 。
该温度下,CO(g) + 2H2(g)  CH3OH(g)的平衡常数
CH3OH(g)的平衡常数
K= 。
相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.CH3OH的平衡浓度 c.达到平衡的时间 d.平衡时气体的密度
(4)以CH3OH为燃料(以KOH溶液作电解质溶液)可制成CH3OH燃料电池。
①充入CH3OH的电极为 极;
②负极反应的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com