
用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
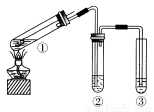
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:填空题
(12 分)钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:
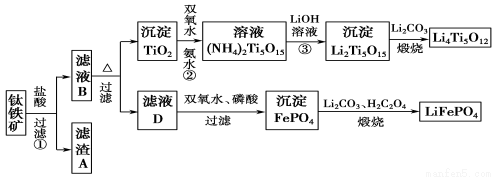
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-===Fe2++TiOCl42-+2H2O。
(1)若在实验室中煅烧固体混合物,会用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有 (填仪器名称)。流程中多次涉及沉淀,则洗涤沉淀的方法是 。
(2)生产中利用滤渣A制备半导体的反应是 。
(3)滤液B中TiOCl42-转化生成TiO2的离子方程式是 。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度有关,反应温度过高时,Ti元素浸出率会下降,其原因是 。
(5)写出由滤液D生成FePO4的离子方程式 。由滤液D制备LiFePO4的过程中,所需双氧水与H2C2O4的物质的量比是 。
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三第三次月考化学试卷(解析版) 题型:选择题
实验室制取少量N2常利用的反应是NaNO2+NH4Cl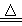 NaCl+N2↑+2H2O,关于该反应的说法正确的是
NaCl+N2↑+2H2O,关于该反应的说法正确的是
A.NaNO2是还原剂
B.生成1molN2时转移的电子为6mol
C.NH4Cl中的N元素被氧化
D.N2既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三第三次月考化学试卷(解析版) 题型:选择题
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转化技术;
④田间焚烧秸秆;⑤推广使用节能环保材料。
A.①③⑤ B.②③⑤ C.①②④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三10月月考化学试卷(解析版) 题型:选择题
已知氨气极易溶于水,而难溶于有机溶剂CCl4,下列装置中不适宜做NH3的尾气吸收装置的是( )
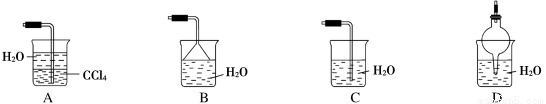
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三10月月考化学试卷(解析版) 题型:选择题
铁片放入下列溶液中,反应时无气体放出,取出后铁片质量减轻,则该溶液是( )
A.稀硫酸 B.浓盐酸 C.AgNO3 D.Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三10月月考化学试卷(解析版) 题型:选择题
将下列各种单质投入或通入CuSO4溶液中,能产生铜单质的是( )
A.Fe B.Na C.H2 D.Ag
查看答案和解析>>
科目:高中化学 来源:2015届吉林省吉林市高三第一次摸底考试化学试卷(解析版) 题型:选择题
CO(g)+NO2(g)  CO2(g)+NO(g) △H<0,若其他条件不变,只改变下列条件,能使混合气体颜色变深的是
CO2(g)+NO(g) △H<0,若其他条件不变,只改变下列条件,能使混合气体颜色变深的是
A.降低温度 B.增大压强 C.增大CO的浓度 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2015届北京理工附中高三第一次月考化学试卷(解析版) 题型:选择题
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是
A、均减半 B、均加倍 C、均增加1 mol D、均减少1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com