
����Ŀ������������ȷ���ǣ� �� 
A.Cu2O��һ�ְ뵼����ϣ�������ɫ��ѧ������Ƶ���ȡCu2O�ĵ���ʾ��ͼ��ͼһ��ʾ��ʯī�缫�ϲ���������ͭ�缫����������Ӧ
B.ͼһ��ʾ����0.1mol����ת��ʱ����0.1mol Cu2O����
C.ͼ��װ���з�����Cu+2Fe3+�TCu2++2Fe2+ �� X���Ǹ�����Y�����Ͽ�����ͭ
D.��ͼ�������ŵ������Ǵ��ݵ����ά�ֵ��ƽ�⣬Fe3+�������Ž�������ձ���
���𰸡�A
���������⣺A�����ݵ���ܷ�ӦΪ2Cu+H2O�TCu2O+H2������֪������ͭΪ�������ϣ�Cuʧ���ӷ���������Ӧ��ʯīΪ�������ϣ������������ӵõ���������������A��ȷ��B��2molCuʧȥ2mol��������1molCu2O�����Ե���0.1mol����ת��ʱ����0.05mol Cu2O���ɣ���B����
C����֪Cu+2Fe3+�TCu2++2Fe2+ �� ���ԭ�����Cuʧ������������Cu������ͭ��Һ�У���XΪCu����YΪ�����Ա�ͭ���Ľ�����ķǽ���������������C����
D��ԭ������������������ƶ������ŵ������Ǵ��ݵ����ά�ֵ��ƽ�⣬�Ҳ�Ϊ����������Fe3+���Ҳ��ձ��в������ƶ�����D����
��ѡA��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NF3����һ�����͵��Ӳ��ϣ����ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ����У�HF��NO��HNO3 �� �����Ҫ��ش��������⣺
��1����Ӧ�����У��������뱻��ԭ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ ��
��2��д���÷�Ӧ�Ļ�ѧ����ʽ �� ����Ӧ������0.2mol HNO3 �� ת�Ƶĵ�����ĿΪ����
��3��NF3��һ����ɫ���������壬��һ��NF3�ڿ�����й©���������ڷ��֣����жϸ�����й©ʱ�������� ��
��4��һ��NF3й©��������NaOH��Һ���ܵķ���������Ⱦ��������NaNO2��NaF��H2O�⣬���϶������ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ж���ȷ����
A.�������е���Ԫ��һ���� - 2��B.��������������ǽ���������
C.��ѧ��ֻ�����ھ�����D.������������м��Dz�������600
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����Ź����ߴӰ������̴���ͭ��ַ�У����ֵ�ʱұ��ͭ����Ҫ����ԭ���ǿ�ȸʯ��Cu2��OH��2CO3������Ҫȼ����ľ̿��ұ���¶ȹ�����1000�����ң�
���϶���������������������������м��������������Ϊͭ����������������������ͭһ������ʣ�����ȸʯ���������еô���Һ����������Ͷ�����Һ�м��ɵ�ͭ��
��1���������������Ϳ�ȸʯ��ˮ���Է����У��ж���ȷ����__________
A��ǰ�߿��ܣ��������� B��ǰ�����ܣ����߿���
C�����߾����� D�����߾�����
��2���Կ�ȸʯΪԭ�ϵ�ұ�������У����ִ���ѧ�Ĺ������ӣ������漰�Ļ�ѧ��Ӧ��__________
��Cu2��OH��2CO3![]() 2CuO+CO2��+H2O
2CuO+CO2��+H2O
��2CuO+C ![]() 2Cu+CO2��
2Cu+CO2��
��CuO+CO ![]() Cu+CO2
Cu+CO2
��CO2+C ![]() 2CO
2CO
A���٢� B���٢� C���٢ڢ� D���٢ڢ�
��3������2�����ĸ���Ӧ�У����������ֻ�����Ӧ���͵��У�����ţ���ͬ��__________��������������ԭ��Ӧ����__________��
��4�����϶��У������ܽ��ȸʯ������ϡ���ᣬд���ô˷���ұ��ͭ�Ļ�ѧ����ʽ ______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʢ��1Lˮ�ļס��ҡ��������ĸ��ձ��ڷֱ��������ʵ�����Na��Na2O��Na2O2��NaOH��������ȫ�ܽ���ձ������ʵ�����������С˳���ǣ� ��
A. �ף��ң������� B. �����ף��ң���
C. �ף������ң��� D. �����ף�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���淴ӦmA��g��+nB��g��pC��g�������ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��t���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ���B%�Ĺ�ϵ���ߣ������߷����������ж���ȷ���ǣ� �� 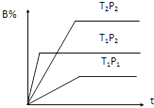
A.T1��T2��P1��P2��m+n��p����H��0
B.T1��T2��P1��P2��m+n��p����H��0
C.T1��T2��P1��P2��m+n��p����H��0
D.T1��T2��P1��P2��m+n��p����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ��������������Na2SO4��ˮ��ԭ����ͼ��ʾ�����ö��Ե缫��ab��cd��Ϊ���ӽ���Ĥ����ֱ���糡�������£���Ĥ�м��Na+��SO42����ͨ�����ӽ���Ĥ�������˸��������ӱ��赲���ܽ����м���ң�����������ȷ���ǣ� �� 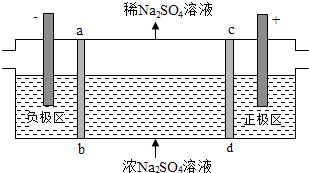
A.ͨ����м���ҵ�SO42������������Ǩ�ƣ���������ҺpH����
B.�÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ
C.������ӦΪ2H2O��4e��=O2+4H+ �� ��������ҺpH����
D.����·��ͨ��1mol���ӵĵ���ʱ������0.5mol��O2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����2L�����ܱ���������̬����X��Y��Z�����ʵ�����ʱ��仯�IJ������������ʾ��
T/min | n��X��/mol | n��Y��/mol | n��Z��/mol |
0 | 0.80 | 1.00 | 0 |
1 | 0.70 | 0.80 | |
5 | 0.70 | ||
9 | 0.40 | ||
10 | 0.40 | 0.80 |
��1��д���÷�Ӧ�Ļ�ѧ����ʽ
��2����Ӧ���е�10min��X��ת����Ϊ �� 0��5min��Y��ƽ����Ӧ����Ϊ
��3������T��ʱ�÷�Ӧ��ƽ�ⳣ��K=
��4��T��������ܱ�������ͨ��һ������X��Y��Z����Ӧ��ijʱ�̲��X��Y��Z�����ʵ����ֱ�Ϊ1.00mol��0.50mol��1.60mol�����ʱ���淴Ӧ���ʴ�С��v��v��������ڡ��������ڡ�����С�ڡ���
��5������10min��t3��t5ʱ�̷ֱ�ı�÷�Ӧ��ijһ��Ӧ�������õ�X��Z�����ʵ�������Ӧ������ʱ��Ĺ�ϵ��ͼA��B��ʾ�� 
��10minʱ�ı�ķ�Ӧ������
��t3ʱ�̸ı�ķ�Ӧ������t5ʱ�̸ı�ķ�Ӧ������ �� ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.���ӻ�������һ�����н���Ԫ��B.ԭ�Ӿ����ۻ�Ҫ�ƻ����ۼ�
C.���ɷ��Ӿ��������һ�����й��ۼ�D.ֻ�����ӻ������вŴ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com