
����Ŀ���������ȣ�ClO2����һ�ָ�Ч���������е�Ϊ11�森������ط�ĩ�������60��ʱ��Ӧ�����ɶ������ȵ����ʣ�ʵ��װ����ͼ��ʾ�� 
��1��װ��A�л�Ӧ��װ�IJ��������� �� װ��B�ñ�ˮԡ��ԭ���� ��
��2��װ��A�в�����K2CO3��ClO2��CO2�ȣ���д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����ʵ������У�װ��C��������ClO2��NaOH��Һ��Ӧ�����������Σ������ʵ���֮��Ϊ1��1������һ��ΪNaClO2 �� д��װ��C���������������ε����ӷ���ʽ�� �� �ڱ�����Һ���¶ȵ���38��ʱ��������NaClO2 �� 3H2O�����¶ȸ���38��ʱ��������NaClO2 �� �벹���NaClO2��Һ���Ƶ�NaClO2����IJ������裺
a����b����c��ϴ�ӣ�d�����
��4�����ɲ��������˫��ˮ��ԭ�������Ʊ�ClO2 �� ��H2O2����ԭ���Ʊ�ClO2���ܻ�ӭ������Ҫԭ���� ��
���𰸡�
��1���¶ȼƣ������¶�������Ϊ��̬
��2��2KClO3+H2C2O4 ![]() K2CO3+CO2��+2ClO2��+H2O
K2CO3+CO2��+2ClO2��+H2O
��3��2ClO2+2OH��=ClO2��+ClO3��+H2O�������ᾧ�����ȹ���
��4��H2O2����ԭ��ʱ��������ΪO2 �� ����������ԭ��ʱ��������Cl2 �� ��Ⱦ����
���������⣺��1���������ȣ�ClO2���е�Ϊ11�棬������ط�ĩ�������60��ʱ��Ӧ�����ɶ������ȵ����ʣ�װ��A���������¶ȿ���װ�ã���װ��A�л�Ӧ��װ�IJ����������¶ȼƣ�װ��B�ñ�ˮԡ��ԭ����ClO2�ķе㣺11.0�棬�е�ͣ��ñ�ˮ����ʹClO2����ΪҺ�壬�ռ����Թ��л����¶�������Ϊ��̬���Դ��ǣ��¶ȼƣ������¶�������Ϊ��̬����2��KClO3�Ͳ��ᷢ��������ԭ��Ӧ����ClO2��K2CO3��CO2��H2O����Ӧ�Ļ�ѧ����ʽΪ2KClO3+H2C2O4 ![]() K2CO3+CO2��+2ClO2��+H2O�����Դ��ǣ�2KClO3+H2C2O4
K2CO3+CO2��+2ClO2��+H2O�����Դ��ǣ�2KClO3+H2C2O4 ![]() K2CO3+CO2��+2ClO2��+H2O����3���ٸ���ClO2�ڼ���Һ�з���᪻�����������ͻ�ԭ��������ʵ�����Ϊ1��1����֪Cl�Ļ�������+4��Ϊ+3��+5����ԭ����ΪNaClO2 �� ��������ΪNaClO3 �� ��˻�ѧ����ʽΪ��2ClO2+2OH��=ClO2��+ClO3��+H2O�����Դ��ǣ�2ClO2+2OH��=ClO2��+ClO3��+H2O����NaClO2��Һ���Ƶ�NaClO2����IJ������裺�����ᾧ�����ȹ��ˡ�ϴ�ӡ�������Դ��ǣ������ᾧ�� ���ȹ��ˣ���4�����ɲ��������˫��ˮ��ԭ�������Ʊ�ClO2 �� ��H2O2����ԭ���Ʊ�ClO2���ܻ�ӭ������Ҫԭ����H2O2����ԭ��ʱ��������ΪO2 �� ����������ԭ��ʱ��������Cl2 �� �������������Ⱦ�����Դ��ǣ�H2O2����ԭ��ʱ��������ΪO2 �� ����������ԭ��ʱ��������Cl2 �� ��Ⱦ������
K2CO3+CO2��+2ClO2��+H2O����3���ٸ���ClO2�ڼ���Һ�з���᪻�����������ͻ�ԭ��������ʵ�����Ϊ1��1����֪Cl�Ļ�������+4��Ϊ+3��+5����ԭ����ΪNaClO2 �� ��������ΪNaClO3 �� ��˻�ѧ����ʽΪ��2ClO2+2OH��=ClO2��+ClO3��+H2O�����Դ��ǣ�2ClO2+2OH��=ClO2��+ClO3��+H2O����NaClO2��Һ���Ƶ�NaClO2����IJ������裺�����ᾧ�����ȹ��ˡ�ϴ�ӡ�������Դ��ǣ������ᾧ�� ���ȹ��ˣ���4�����ɲ��������˫��ˮ��ԭ�������Ʊ�ClO2 �� ��H2O2����ԭ���Ʊ�ClO2���ܻ�ӭ������Ҫԭ����H2O2����ԭ��ʱ��������ΪO2 �� ����������ԭ��ʱ��������Cl2 �� �������������Ⱦ�����Դ��ǣ�H2O2����ԭ��ʱ��������ΪO2 �� ����������ԭ��ʱ��������Cl2 �� ��Ⱦ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���Ԫ����������ѧϰ���о�������ʵ���ж��зdz���Ҫ�����á��±���Ԫ�����ڱ�ǰ�����ڵ�һ���֣��г��ˢ���������Ԫ�������ڱ��е�λ�á�
�� | �� | �� | |||
�� | �� | �� | �� |
��ش�
��1����������Ԫ�ص�����Ϊ______
��2������Ԫ���У��ǽ�������ǿ��Ԫ����______(��Ԫ�ط���)������������ˮ����������ǿ����_______(�ѧʽ)����������ϼ���������ϼ۵Ĵ�����Ϊ4��Ԫ����_______(��Ԫ�ط���)��
��3����������������ӦԪ����ԭ�Ӱ뾶��С����______(��Ԫ�ط���)�������Ӱ뾶������______(�����ӷ���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��̽��SO2���廹ԭFe3+��I2 �� ����ʹ�õ�ҩƷ��װ������ͼ��ʾ�� 
��1��װ��C�������� ��
��2����Ҫ��FeSO4��Һ���FeSO47H2O���壬������е�ʵ��������裺�������ˡ�ϴ�ӡ���Ȼ���
��3��������������С��ͬѧ��ΪSO2 �� FeCl3��Һ����������ԭ��Ӧ�� ��д��SO2��FeCl3��Һ��Ӧ�����ӷ���ʽ��
����д������A�ձ�����Fe2+���ɵIJ���������
�۸�С��ͬѧ��C�ձ���Ӧ�����Һ�м��������ữ��BaCl2��Һ�������ְ�ɫ����������֤����Ӧ������SO42�� �� ��������������������������������� ��
��4���ܱ���I���Ļ�ԭ������SO2�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǿ��淴ӦX2+3Y22Z�ڷ�Ӧ�����еķ�Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ���ߣ�����������ȷ���ǣ� �� 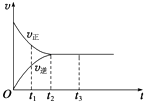
A.t1ʱ��ֻ��������Ӧ
B.t2ʱ����Ӧ�ﵽ��
C.t2��t3 �� ��Ӧ���ٷ���
D.t2��t3 �� �����ʵ�Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��������������Ӧ�ù㷺��ij�������ú��������ķ�ͭ��Ϊԭ������������������ͼ�� 
��1��д������ʱͭ��ϡ���ᡢϡ���ᷴӦ��������ͭ�Ļ�ѧ����ʽ�� ��
��2��ȡ��������Ϊ��ȷ��Fe3+�Ƿ��������ļ��鷽���� ��
��3������c�� ��
��4������a���Ա�ѭ�����ã��û�ѧ����ʽ��ʾ����a��ѭ�����õ�ԭ��Ϊ 2NO+O2�T2NO2�� ��
��5��һ���¶��£�����ͭ���ȷֽ�����CuO��SO2���塢SO3�����O2���壬��n��SO3����n��SO2��=1��2��д������ͭ���ȷֽ�Ļ�ѧ����ʽ�� ��
��6��ijͬѧ�������ͼ��ʾ��ʵ��װ�÷ֱ�ⶨ���ɵ�SO2��SO3�����������O2����������������в�����֮������˵�����ɣ� �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50 mL 0.3 mol/L Fe2(SO4)3��Һ��ˮϡ�͵�500 mL��ϡ�ͺ���Һ��SO42�����ʵ���Ũ��Ϊ
A.0.01 mol/LB.0.03 mol/LC.0.06mol/LD.0.09 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25.4gij���۽������Ȼ���RCl2�к���0.4mol��Cl-����R��Ԫ�ط���Ϊ
A. Mg B. Ca C. Fe D. Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H��C��N��O��Na��Fe��Cu�dz���������Ԫ�ء�
��1��N��Na+��Fe3+��Cu2+��������̬�ĺ�������Ų�ʽ��δ�ɶԵ�����������____________��
��2�����ݼ۲���ӶԻ��������ж����з��ӻ������пռ乹����V�ε���______����д��ţ���
a. ![]() b.
b. ![]()
c. ![]() d.
d. ![]()
��3������(CN)2�м����֮��ļн�Ϊ180�������жԳ��ԣ�������ÿ��ԭ������������8�����ȶ��ṹ����ṹʽΪ___________��1�������к���_________��������
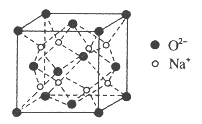
��4��O��Na�γɵ�һ��ֻ�������Ӽ������ӻ�����侧���ṹ��ͼ�������ӻ�����Ļ�ѧʽΪ_____________����֪�þ������ܶ�Ϊ��g/cm3�������ӵ�����ΪNA�����߳�![]() _______cm�����ú�����NA�Ĵ���ʽ��ʾ��
_______cm�����ú�����NA�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ͼ��ʾת����ϵ(X����±��)��˵���������

A. ��H3<0
B. ��H1=��H2+��H3
C. ��Cl��Br��I��˳��H2��������
D. ��H1ԽС��HXԽ�ȶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com