
¶ą²ŹĖ®ÄąµÄĢķ¼Ó¼ĮŹĒCoCl2-6H2O”£¹¤¶ØŹĒŅŌŗ¬īÜ·ĻĮĻ£Øŗ¬ÉŁĮæFe”¢AlµČŌÓÖŹÖĘČ”CoCl2”¤6H2OµÄŅ»ÖÖŠĀ¹¤ŅÕĮ÷³ĢČēĻĀĶ¼£ŗ
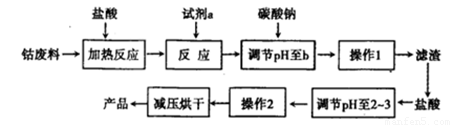
ŅŃÖŖ£ŗ¢ŁīÜÓėŃĪĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCo+2HCl CoCl2+H2”ü
¢ŚCoCl2”¤6H2OČܵć86oC£¬Ņ×ČÜÓŚĖ®”¢ŅŅĆŃµČ£»³£ĪĀĻĀĪȶØĪŽ¶¾£¬¼ÓČČÖĮ110oC”«120OCŹ±£¬Ź§Č„½į¾§Ė®±ä³ÉÓŠ¶¾µÄĪŽĖ®ĀČ»ÆīÜ”£
¢Ū²æ·ÖŃōĄė×ÓŅŌĒāŃõ»ÆĪļŠĪŹ½³ĮµķŹ±ČÜŅŗµÄpH¼ūĻĀ±ķ£ŗ
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÉĻŹöĮ÷³ĢÖŠµÄŹŌ¼ĮaæÉÄÜĪŖ £»Ęä×÷ÓĆŹĒ £»
£Ø2£©¼ÓČėĢ¼ĖįÄʵ÷½ŚpHÖĮb£¬bµÄ·¶Ī§ŹĒ £»
|
³ĮµķĪļ |
Fe£ØOH£©3 |
Fe£ØOH£©2 |
Co£ØOH£©2 |
Al£ØOH£©3 |
|
æŖŹ¼³Įµķ£ØpH£© |
2.3 |
7.5 |
7.6 |
3.4 |
|
ĶźČ«³Įµķ£ØpH£© |
4.1 |
9.7 |
9.2 |
5.2 |
£Ø3£©²Ł×÷1ŹĒ £»ĀĖŌüµÄ³É·ÖĪŖ £»
£Ø4£©²Ł×÷2µÄ¹ż³ĢĪŖÕō·¢ÅØĖõ”¢ ŗĶ¹żĀĖ”£
£Ø5£©ÖʵƵÄCoCl2”¤6H2OŠč¼õŃ¹ŗęøɵÄŌŅņŹĒ ”£
£Ø1£©H2O2(»ņC12)Ńõ»Æ¶ž¼ŪĢśĄė×Ó
£Ø2£©5.2”«7.6
£Ø3£©¹żĀĖ Fe(OH)3ŗĶA1(OH)3
£Ø4£©ĄäČ“½į¾§
£Ø5£©½µµĶŗęøÉĪĀ¶Č£¬·ĄÖ¹²śĘ··Ö½ā(Ź§Č„½į¾§Ė®)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©“Ó±ķøńŗĶ¹¤ŅÕĮ÷³Ģ·ÖĪö£¬ŌŚµ÷ÕūpHĒ°£¬Ó¦½«Fe2+Ńõ»ÆĪŖFe3+£¬ĖłŅŌÓ¦¼ÓŃõ»Æ¼Į£»£Ø2£©“Ó±ķøńÖŠø÷ĪļÖŹ³ĮµķµÄpH£¬Šč½«Al3+”¢Fe3+³Įµķ¶ųCo2+²»³Įµķ£¬“Ó¶ųµĆµ½ĖłŠčpHµÄ·¶Ī§£»£Ø5£©²ÉÓƵĶŃ¹µÄÖ÷ŅŖŌŅņŹĒ·ĄÖ¹·Ö½ā”£
æ¼µć£ŗ漲鹤ŅÕĮ÷³ĢÖŠµÄŹµŃé²Ł×÷¼°ĪļÖŹŠŌÖŹ£¬æ¼²éæ¼ÉśŌĖÓĆ»ÆѧÖŖŹ¶½ā¾öŹµ¼ŹĪŹĢāµÄÄÜĮ¦”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
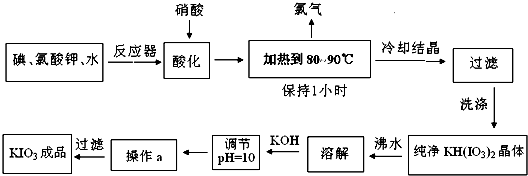
| ĪĀ¶Č | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100gĖ® | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KOH g/100gĖ® | 49.2 | 50.8 | 52.8 | 59.8 | 62.4 | 78.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013½ģÕć½Ź”ŗ¼ÖŻµŲĒųĘߊ£ø߶žĻĀѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶Ō±½¶ž·ÓŹĒÉćÓ°ŅµÖŠ³£ÓĆĻŌÓ°¼Į£¬ĖüŌŚĖ®ÖŠµēĄė³öµÄŅõĄė×Ó¶ŌŅŃĘŲ¹āµÄAgBrÓŠĻŌÓ°×÷ÓĆ£¬ÓŠ¹Ų±ä»ÆæɱķŹ¾ĪŖ£ŗ
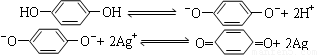
ŌņŌŚŅŌ¶Ō±½¶ž·ÓĪŖÖ÷ŅŖ³É·ÖµÄĻŌÓ°ŅŗÖŠ£¬ÄÜŹ¹ĻŌÓ°ĖŁ¶ČĆ÷ĻŌ¼ÓæģµÄĢķ¼Ó¼ĮŹĒ
”” A£®KBr B£®Na2CO3 C£®CH3COOH D£®H2O
”¾½āĪö”æŅŖŹ¹ĻŌÓ°ĖŁ¶ČĆ÷ĻŌ¼Óæģ£¬ŌņĘ½ŗā±ŲŠėĻņÕż·“Ó¦·½ĻņŅʶÆĢ¼ĖįÄĘÄÜĻūŗÄĒāĄė×Ó£¬“ŁŹ¹¶Ō±½¶ž·ÓµÄµēĄėĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌ“š°øŹĒB”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com