

| A.X、Y、Z的含氧酸的酸性依次增强 |
| B.W元素形成的单核阴离子还原性强于X |
| C.W、X、Y的原子半径依次增大 |
| D.W与氢元素形成的化合物中可能含有非极性键 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.W2Y溶液显中性 |
| B.W与Z形成的化合物中不含有离子键 |
| C.1mol元素Z的单质与足量的W的最高价氧化物对应的水化物的溶液反应,转移1mol电子 |
| D.W、X的单质通常是电解其氧化物得到 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
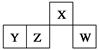
| A.原子半径:rW>rZ>rY>rX |
| B.含Y元素的盐溶液一定显酸性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B.YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 |
| C.原子半径:Z<Y<W,而简单离子半径:W<Y<Z |
| D.W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.质子数c>b |
| B.原子半径X<W |
| C.氢化物的稳定性H2Y>HZ |
| D.离子的还原性Y2->Z- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com