
| A. | Z2+能促进水的电离 | |
| B. | 常见单质的熔点:X>Z>Y | |
| C. | 若元素R的某种微粒R2-,则R不一定与Y同主族 | |
| D. | Y与W组成的二元化合物是制耐高温坩埚的常用材料 |
分析 X、Y、Z、W的原子序数依次递增的短周期元素,已知X元素能组成自然界中最坚硬的单质,则X为C元素,X与W同主族,则W为Si,Y2-与Z2+与具有相同的电子层结构,可推知Y为O元素,Z为Mg,结合元素化合物性质解答.
解答 解:X、Y、Z、W的原子序数依次递增的短周期元素,已知X元素能组成自然界中最坚硬的单质,则X为C元素,X与W同主族,则W为Si,Y2-与Z2+与具有相同的电子层结构,可推知Y为O元素,Z为Mg.
A.Mg2+发生水解,促进水的电离,故A正确;
B.X常见单质为金刚石等,金刚石属于原子晶体,Mg的单质属于金属晶体,氧气属于分子晶体,故常见单质的熔点:金刚石>Mg>氧气,故B正确;
C.若元素R的某种微粒R2-,则R与Y(氧)同主族,故C错误;
D.Y与W组成的二元化合物为二氧化硅,是制耐高温坩埚的常用材料,故D正确.
故选:C.
点评 本题考查了原子结构与元素周期律的关系,正确推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,熟练掌握元素化合物知识.


科目:高中化学 来源: 题型:选择题
| A. | -283.01KJ/mol | B. | +172.51 KJ/mol | C. | +283.01KJ/mol | D. | -504.01 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
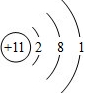 ,YX3的电子式为
,YX3的电子式为 (用元素符号表示).
(用元素符号表示). 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1 | B. | 2mol•L-1 | C. | 3mol•L-1 | D. | 4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .该阳离子中存在的化学键有共价键.
.该阳离子中存在的化学键有共价键. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com