
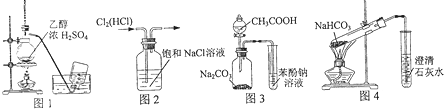
| A、利用图1装置制备乙烯 |
| B、利用图2装置除去Cl2中的HCl |
| C、利用图3装置证明酸性:CH3COOH>H2CO3>苯酚 |
| D、利用图4装置探究NaHCO3的热稳定性 |


科目:高中化学 来源: 题型:
 (1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式| 1 |
| 2 |
| t/K | 298 | 398 | 498 | … |
| K/(mol.L-1)-2 | 4.1X106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组用右图进行实验,试回答下列问题.
某课外活动小组用右图进行实验,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若存在简单阴离子R-,则R一定属于ⅦA族 |
| B、若存在简单阴离子R2-,则R一定属于VIA族 |
| C、若存在简单阳离子M+,则M一定属于IA族 |
| D、若存在简单阳离子M2+,则M一定属于ⅡA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、23.5g |
| B、11.5g |
| C、23.0g |
| D、19.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①③④⑤ |
| C、①②④⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极的电极反应式为:Al-3e-=Al3+ |
| B、该电池可以用NaOH或KOH水溶液作为电解质溶液 |
| C、该电池的电池总反应式为:2Li+FeS=Li2S+Fe |
| D、充电时,阴极发生的电极反应式为:Li2S+Fe-2e-=2Li++FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3- |
| B、导致易拉罐又鼓起来的反应是:Al3++3HCO3-═Al(OH)3+3CO2↑ |
| C、若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
| D、上述过程中总共发生了3个反应,且反应结束后的溶液显碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com