
(10分)五种元素的原子电子层结构如下:
| A.1s22s1; | B.1s22s22p4; | C.1s22s22p6; | D.1s22s22p63s23p2 E.[Ar]3d104s1。(用元素符号作答) |
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届福建省高二期末考试化学试卷(解析版) 题型:填空题
(12分)
(1)五种元素的原子电子层结构如下:A:1s22s22p63s2 B:1s22s22p63s23p63d54s2 C:1s22s1 D:1s22s22p63s23p2 E:1s22s22p6。请回答:(填元素符号)
元素的电负性最大, 元素原子的第一电离能最小, 元素最可能生成具有催化性质的氧化物。
(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”, 钛有4822Ti和5022Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 ,按电子排布Ti元素在元素周期表分区中属于 区元素。
(3)A、B两种元素的电离能数据如下(kJ·mol—1):
|
电离能/kJ•mol-1 |
I1 |
I2 |
I3 |
I4 |
|
A |
577 |
1817 |
2745 |
11578 |
|
B |
738 |
1451 |
7733 |
10540 |
化合价是元素的一种性质。由A、B的电离能数据判断,A通常显 价,B显 价。
(4)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示。请将图中你认为是配位键的斜线上加上箭头。
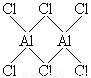
(5)假设原子晶体SiO2中Si原子被铝原子取代,不足的价数由钾原子补充。当有25%的硅原子被铝原子取代时,可形成正长石。则正长石的化学组成为 。
(6)CO2与SiO2比较沸点相差很大的原因是 。
查看答案和解析>>
科目:高中化学 来源:2013届山西大同实验中学高二下学期期中考试化学试卷(解析版) 题型:填空题
(10分)五种元素的原子电子层结构如下:A.1s22s1 ;B.1s22s22p4 ;C.1s22s22p6; D.1s22s22p63s23p2 E.[Ar]3d104s1。(用元素符号作答)
(1)元素的第一电离能最大的是 ;
(2)属于过渡元素的是 ;
(3)元素的电负性最大的是 ;
(4)上述元素之间能形成X2Y型化合物的化学式是 、
查看答案和解析>>
科目:高中化学 来源:2013届福建师大附中高二下学期期中考试化学试卷(解析版) 题型:填空题
(14分)(1)五种元素的原子电子层结构如下:A:1s22s22p63s23p63d54s2、B:1s22s22p63s2、C:1s22s22p6、D:1s22s22p63s23p2、E:1s22s1。请回答:(填元素符号)
元素的电负性最大, 元素原子的第一电离能最大, 元素最可能生成具有催化性质的氧化物。
(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”, 钛有4822Ti和5022Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 ,按电子排布Ti元素在元素周期表分区中属于 区元素。
(3)A、B两种元素的电离能数据如下(kJ·mol—1):
|
|
I1 |
I2 |
I3 |
I4 |
|
A |
738 |
1451 |
7733 |
10540 |
|
B |
577 |
1817 |
2745 |
11578 |
化合价是元素的一种性质。由A、B的电离能数据判断,A通常显 价,B显 价。
(4)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示。请将图中你认为是配位键的斜线上加上箭头.
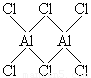
(5)假设原子晶体SiO2中Si原子被铝原子取代,不足的价数由钾原子补充.当有25%的硅原子被铝原子取代时,可形成正长石.则正长石的化学组成为
(6)NH3极易溶于水其原因是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com