
(8分)右图中电极a、b为Fe物件和Ag片,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336ml(标准状况)气体。回答:
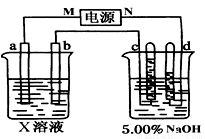
(1)直流电源中,M为_________________极。
(2)欲在Fe物件上镀上一薄层Ag,
①Fe物件应为_________极,(填a或b)
②Fe物件增重_________g。
(3)X溶液为____________,其浓度____________,(填“增大”“减小”或“不变”)
(4)若NaOH溶液的质量分数由5.00%变为5.02%,列式计算原NaOH溶液的质量。
科目:高中化学 来源: 题型:
(8分)右图中电极a、b为Fe物件和Ag片,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336ml(标准状况)气体。回答:
(1)直流电源中,M为_________________极。
(2)欲在Fe物件上镀上一薄层Ag,
①Fe物件应为_________极,(填a或b)
②Fe物件增重_________g。
(3)X溶液为____________,其浓度____________,(填“增大”“减小”或“不变”)
(4)若NaOH溶液的质量分数由5.00%变为5.02%,列式计算原NaOH溶液的质量。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省南昌二中高二上学期期末考试化学试卷 题型:填空题
(8分)右图中电极a、b为Fe物件和Ag片,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336ml(标准状况)气体。回答: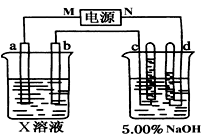
(1)直流电源中,M为_________________极。
(2)欲在Fe物件上镀上一薄层Ag,
①Fe物件应为_________极,(填a或b)
②Fe物件增重_________g。
(3)X溶液为____________,其浓度____________,(填“增大”“减小”或“不变”)
(4)若NaOH溶液的质量分数由5.00%变为5.02%,列式计算原NaOH溶液的质量。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省德阳市高三第一次诊断性考试化学试卷 题型:填空题
(12分)A、B、C、D、E五种均为短周期元素,原子序数依次增大。A元素原子最外层电子数是核外电子层数的3倍,A与D同主族,A和D可形成化合物X’X可以使溴水褪色。A元素的单质和C元素的单质化合可生成Y, Y晶体中无分子,也无A、C的离子。A、B元素的单质一定条件下反应生成化合物M,D、B元素的单质反应生成化合物N,化合物M和化合物N的相对分子质量相等,且馅色反应均呈黄色。
请回答下列问题:
(1) 元素C的气态氢化物是________分子(填写“极性”或“非极性”)。
(2) B2D2的电子式是________________
(3) X可以使溴水褪色,该反应的离子方程式是________________________。
(4) 化合物M与化合物N的水溶液反应,若氧化剂与还原剂物质的量之比为1: 1,该反应的离子方程式是________
(5) 右图是BE晶体的一个“晶胞结构”示意图。下列说法正确的是________________。

A. 与B+距离相等且最近的E_共有6个
B. —个BE晶胞中含有1个B +和1个E_
C. 与B+距离相等且最近的B +有8个
D. 与B+距离相等且最近的构成的空间结构是正八面体
(6) 将原子序数介于B、C两元素之间的单质、单质B与水反应所得的溶液构成原电池,负极的电极反应式是:O
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)(1)(4分)有一部分化学反应的反应热测定起来很困难,我们可以根据盖斯定律计算获得。如同素异形体之间的转化反应热数值小且转化慢,测定较困难。已知:
①![]() 白磷
白磷![]()
![]()
②![]() 红磷
红磷![]()
![]()
写出白磷转化为红磷的热化学方程式:__________________________。则对应下
列化学反应过程中的能量变化图,能正确反映出由白磷转化为红磷的是_____________。

(2)(8分)有右图装置:回答下列问题:
①装置A是_______池,B是_______池。
②装置A中的Zn极是_______极,Cu极上
的电极反应方程式为:__________________。
③锌与铁组成的合金在潮湿的空气中,
锌被腐蚀而另一种金属被保护,这种保护方法叫
做_______,正极反应式为__________________ 。
![]() ④装置B中是浓度均为
④装置B中是浓度均为![]() 的NaCl、CuSO
的NaCl、CuSO![]() 混合溶液,溶液体积为500mL。当装置A中Zn棒质量减少32.5g时,C
混合溶液,溶液体积为500mL。当装置A中Zn棒质量减少32.5g时,C![]() 上质量增加____________g;
上质量增加____________g;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com