
宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2====2X+2H2O,下列说法中正确的是( )
A.X的化学式为AgS
B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂
D.每生成1 mol X,反应转移2 mol电子
科目:高中化学 来源: 题型:
对σ键的认识不正确的是( )
A.σ键不属于共价键,是另一种化学键
B.S-Sσ键与S-Pσ键的对称性相同
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、硫的含量影响钢铁性能,碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2。
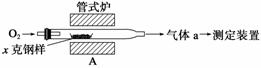
①气体a的成分是________________。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2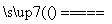 1________+3________。
1________+3________。
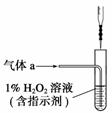
(2)将气体a通入测硫装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式
________________________________________________________________________
________________________________________________________________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液,若消耗1 mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。
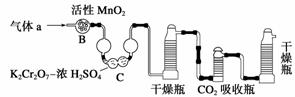
①气体a通过B和C的目的是_______________________________________________。
②计算钢样中碳的质量分数,应测量的数据是___________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组的同学在获得了如下资料的情况下,利用下面的装置来探究二氧化氮与碳酸氢钠溶液反应的产物及反应的机理。
资料:①亚硝酸是一种弱酸,酸性较碳酸酸性强;
②亚硝酸不稳定,很易分解:3HNO2===HNO3+2NO↑+H2O。
实验步骤如下:
①检查装置气密性;
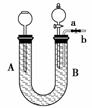
②在U形管中盛满蒸馏水,从b处通入二氧化氮气体,在U形管的B处得到无色气体,打开分液漏斗活塞,使少量气体进入分液漏斗,在分液漏斗中看到有红棕色气体;
③在U形管中盛满饱和碳酸氢钠溶液,从b处通入二氧化氮气体,在U形管的B处也得到无色气体,打开分液漏斗活塞,使少量气体进入分液漏斗,在分液漏斗中却看不到红棕色气体;
④将③中B处无色气体通过导管b通入足量澄清石灰水中有白色沉淀生成;
⑤将U形管中盛满氢氧化钠溶液,从b处通入二氧化氮时在B处得不到任何气体。
请回答下列各题:
(1)检查装置气密性的方法为__________________________________________________。
(2)在②中B处得到的无色气体是__________;用两个化学方程式表示二氧化氮与水反应的化学反应机理:_________________________________________________________________。
(3)在③中B处得到的无色气体(单一纯净)是________;只得到该无色气体的原因是________________________________________________________________________。
(4)取出③中得到的溶液,加入足量稀盐酸,预测可观察到的现象________________________________________________________________________。
(5)写出⑤中发生反应的化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中只存在OH-、Cl-、N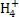 、H+四种离子,下列说法不正确的是( )
、H+四种离子,下列说法不正确的是( )
A.若溶液中c(N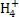 )=c(Cl-),则该溶液一定显中性
)=c(Cl-),则该溶液一定显中性
B.若溶液中c(N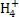 )>c(Cl-)>c(OH-)>c(H+),则溶液中一定含有NH4Cl和NH3·H2O
)>c(Cl-)>c(OH-)>c(H+),则溶液中一定含有NH4Cl和NH3·H2O
C.若溶液中c(Cl-)>c(N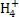 )>c(H+)>c(OH-),则溶液中可能含有NH4Cl或可能含有NH4Cl和HCl
)>c(H+)>c(OH-),则溶液中可能含有NH4Cl或可能含有NH4Cl和HCl
D.若溶液中c(Cl-)>c(H+)>c(N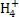 )>c(OH-),则溶液中含有大量的NH4Cl和少量的HCl
)>c(OH-),则溶液中含有大量的NH4Cl和少量的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+3B(g)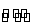 2C(g)+2D(g)在四种不同情况下的反应速率分别为
2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.15 mol·L-1·s-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45 mol·L-1·s-1,
则该反应进行的快慢顺序为( )
A.④>③=②>① B.①>③=②>④
C.④>③>①>②  D.④>③
D.④>③ >②>①
>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示。

(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示) 。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关环境方面的说法不正确的是( )
A.CO能使人中毒的原理是CO能将人体血液中的Fe2+氧化
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,提高空气质量
C.推广可利用太阳能、风能等新能源,发展低碳经济,同时能大大减少对环境的污染
D.PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com