
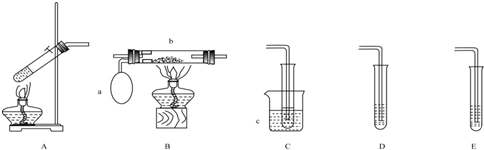
分析 (1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置吸收乙醇,中和乙酸,降低乙酸乙酯溶解度,防止倒吸;A装置液体加热沸腾需要加入碎瓷片/沸石防止暴沸;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,冷却得到液体乙醛.
解答 解:(1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置,不能用连接E,防止倒吸,加入饱和碳酸钠溶液,吸收乙醇,中和乙酸,降低乙酸乙酯溶解度,防止倒吸;A装置液体加热沸腾需要加入碎瓷片/沸石,防止暴沸,A中发生反应为CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:D;饱和碳酸钠溶液;CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,反应的化学方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,冷却得到液体乙醛装置连接为A、B、C,
故答案为:A、B、C;2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查了实验制备和物质性质验证的方法,为高频考点,侧重于学生的分析能力和实验能力的考查,掌握乙醇催化氧化原理和产物性质是解题关键,题目难度中等.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
下列有关“水”的说法中正确的是( )
A.双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境无污染
B.王水是浓盐酸和浓硝酸按体积比1∶3配成的混合物,可溶解Au、Pt
C.氨水能导电,说明氨气是电解质
D.往新制备的氯水中和SO2的水溶液中分别滴入石蕊试液时的现象不同
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
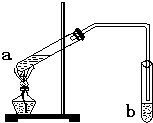 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.请回答下列问题:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
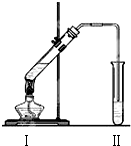 图是实验室制乙酸乙酯的装置.
图是实验室制乙酸乙酯的装置.| 实验 编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL3mol•L-1硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3mL乙醇、2mL乙酸、6mL6mol•L-1盐酸 | 饱和Na2CO3溶液 | 1.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
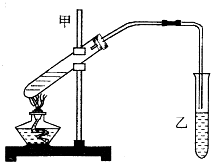 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: CH3COOC2H5+H2O.
CH3COOC2H5+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
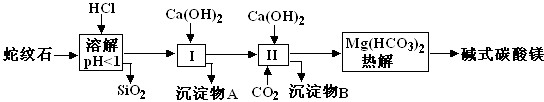
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.3 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
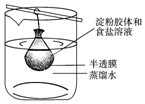 将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )
将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )| A. | 烧杯内液体加入硝酸银溶液后有白色沉淀产生 | |
| B. | 烧杯内液体加入碘水后呈蓝色 | |
| C. | 袋内液体加入硝酸银溶液后不会出现白色沉淀 | |
| D. | 袋内液体加入碘水后不变蓝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com