
现有浓度均为0.1 mol·L-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_____________________ _____________________________________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是__________________________________________________。
(3)已知T ℃,KW=1×10-13,则T ℃________25 ℃(填“>”、“<”或“=”)。在T ℃时将pH=11的NaOH溶液a L与pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=________。
(4)25 ℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=________(填数据);
②若x+y=13,则a/b=________(填数据);
③若x+y>14,则a/b=________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为________(填表达式)。
解析 (1)向溶液中加入酸或碱均能抑制H2O的电离,且溶液中H+或OH-浓度越大,由水电离出的H+浓度越小;盐的水解能促进水的电离,即由水电离出的c(H+)从大到小的顺序为④②③①。(2)二者完全反应生成NaCl和NH3·H2O,NH3·H2O电离使溶液呈碱性,即c(Na+)=c(Cl-)>c(OH-)>c(NH )>c(H+)。(3)温度升高时KW增大,T ℃时KW>1×10-14,即T ℃>25 ℃;NaOH溶液中n(OH-)=0.01 a mol,硫酸中n(H+)=0.1 b mol,根据混合后溶液pH=10,得10-3=
)>c(H+)。(3)温度升高时KW增大,T ℃时KW>1×10-14,即T ℃>25 ℃;NaOH溶液中n(OH-)=0.01 a mol,硫酸中n(H+)=0.1 b mol,根据混合后溶液pH=10,得10-3= ,解得a∶b=101∶9。(4)若两溶液完全中和,则溶液中n(H+)=n(OH-),即10-xa=10y-14b,整理得
,解得a∶b=101∶9。(4)若两溶液完全中和,则溶液中n(H+)=n(OH-),即10-xa=10y-14b,整理得 =10x+y-14,①若x+y=14时,
=10x+y-14,①若x+y=14时, =1;②若x+y=13,则
=1;②若x+y=13,则 =0.1;③若x+y>14,则
=0.1;③若x+y>14,则 =10x+y-14;④两溶液完全中和时,则有
=10x+y-14;④两溶液完全中和时,则有 =10x+y-14即lg
=10x+y-14即lg =x+y-14,解得x+y=14+lg
=x+y-14,解得x+y=14+lg 。
。
答案 (1)④②③① (2)c(Na+)=c(Cl-)>c(OH-)>c(NH )>c(H+) (3)> 101∶9 (4)①1 ②0.1
)>c(H+) (3)> 101∶9 (4)①1 ②0.1
③10x+y-14 ④x+y=14+lg


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是( )
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )
A.丙烷与氯气在光照的作用下的反应 B.乙烯与溴的四氯化溶液的反应
C.乙烯与水的反应 D.乙烯自身生成聚乙烯的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
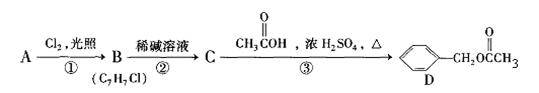 有机物D对花香和果香的香味具有提升作用,故常用于化妆品工业和食品工业。有机物D可以用下面的设计方案合成。
有机物D对花香和果香的香味具有提升作用,故常用于化妆品工业和食品工业。有机物D可以用下面的设计方案合成。
(1)A的结构简式: ,C的名称:
(2)写出下列反应的化学方程式并注明反应类型:
① ,
③ ,
(3)E是D的同系物且相对分子质量比D小14,E的结构可能有 种,请写出结构中无甲基,且水解产物能发生银镜反应的E的一种同分异构体结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.某盐的水溶液呈酸性,该盐一定是强酸弱碱盐
B.弱电解质溶液稀释后,溶液中各种离子浓度一定都减小
C.水的离子积常数KW随着温度的升高而增大,说明水的电离是吸热反应
D.中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值。下列叙述正确的是( )
A.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
B.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA
C.0.1mol·L-1的NH4NO3溶液中氮原子数为0.2NA
D.标准状况下, 22.4L苯中C—H键数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知苯跟一卤代烷在催化剂作用下,可生成苯的同系物。如在催化剂作用下:
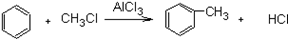 ,苯和下列各组物质合成乙苯最好应选用的是( )
,苯和下列各组物质合成乙苯最好应选用的是( )
A.CH3CH3和Cl2 B.CH2=CH2和HCl C.CH2=CH2和Cl2 D.CH3CH3和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
CH3CH2CH2CH3(g)+6.5O2(g) = 4CO2(g)+5H2O(l) △H =-2878 kJ/mol
(CH3)2CHCH3(g)+6.5O2(g) = 4CO2(g)+5H2O(l) △H =-2869 kJ/mol
下列说法正确的是( )
A.正丁烷的稳定性大于异丁烷
B.异丁烷分子中的碳氢键比正丁烷的多
C.等物质的量的正丁烷能量大于异丁烷能量
D.异丁烷转化为正丁烷的过程是一个放热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度不同压强(P1<P2)下,可逆反应2X(g) 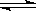 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
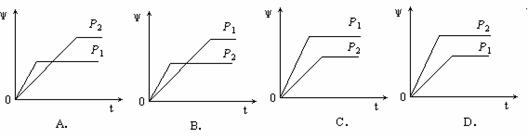
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com