
A.CH4 B.PCl3 C.SiCl4 D.XeF4
科目:高中化学 来源: 题型:
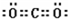
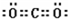
| 284 |
| aNA |
| 284 |
| aNA |
查看答案和解析>>
科目:高中化学 来源:贵州省遵义四中2010-2011学年高二上学期期末考试化学理科试题 题型:013
|
下列分子中,属于含有极性键的非极分子的是 ①CO2 ②P4 ③NH3 ④CH4 ⑤H2O | |
| [ ] | |
A. |
①② |
B. |
①④ |
C. |
④⑤ |
D. |
③⑤ |
查看答案和解析>>
科目:高中化学 来源:2014届江苏泰州二中高二上学期期中考试化学(选修)试卷(解析版) 题型:填空题
(18分)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为是钛(22Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)铁元素位于元素周期表的 区;其基态原子的电子排布式为 。
(2)铜原子的价电子排布式为 ,画出配离子[Cu(H2O)4]2+中的配位键____ _______ 。
(3)二氧化碳分子的立体构形为 形,其中C原子的杂化方式为 杂化,二氧化碳分子中含有 个σ键和 个π键。
(4)氨分子属于 分子(填“极性”或“非极性”);氨极易溶于水最主要的原因是氨分子和水分子之间可以形成 。
(5)下列元素的第一电离能最大的是( )
A.Be B.C C. N D.O
(6)下列分子中,所有原子都满足最外层为8电子结构的是 ( )
A.XeF2 B.BeCl2 C.PCl3 D.CHCl3
(7)下列晶体中,熔点最高的是 。
A.金刚石 B.干冰 C.铝 D.氯化钠

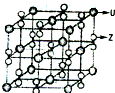
(8)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定;偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如上图,它的化学式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com