
| A. | 28 | B. | 30 | C. | 40 | D. | 42 |
分析 根据C原子、H原子守恒,判断C8H18裂化可能发生的反应情况,根据反应情况判断1molC8H18裂化所得的混合气体的物质的量的范围,再根据极限法计算平均相对分子质量的范围,据此解答.
解答 解:按照题目所给C8H18的裂化产物考虑,C8H18裂化可能发生的反应共有以下几种:
①C8H18→C4H8+C3H6+CH4
②C8H18→C4H8+C2H4+C2H6
③C8H18→2C3H6+C2H6
④C8H18→C3H6+2C2H4+CH4
⑤C8H18→3C2H4+C2H6
以上反应①、②、③是1molC8H18裂化生成3mol混合气体;④、⑤反应是1molC8H18裂化生成4mol混合气体.要得到题目所述的混合气体,按①、②、③反应就可以实现;但是按④、⑤反应并不能得到题目所述的混合气体,至少需要①、②中的一个反应参与或者共同参与,③也有可能同时参与.
这样1molC8H18裂化所得的混合气体的物质的量为:3mol≤n<4mol,所以混合气体的平均摩尔质量$\frac{1mol×114g/mol}{4mol}$<$\overline{M}$≤$\frac{1mol×114g/mol}{3mol}$,
即28.5g/mol<$\overline{M}$≤38g/mol.所以平均相对分子质量为:28.5<$\overline{Mr}$≤38.
故选C.
点评 本题以裂化为载体,考查相对分子质量范围的判断,难度较大,关键判断1molC8H18裂化所得的混合气体的物质的量的范围.


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油裂解产物中有乙烯 | |
| B. | 天然气的主要成分是乙烯 | |
| C. | 芳香烃主要来自于煤干馏产生的煤焦油 | |
| D. | 汽油、煤油、柴油主要来自于石油的常压分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
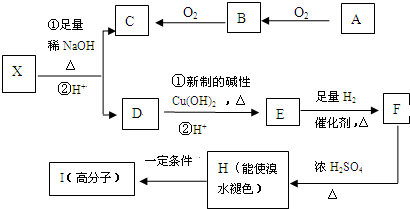
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一定量的氯气通入30 mL浓度为10.0mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系,n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 | |
| B. | 实验室可以配制一种仅含Al3+、K+、SO42-、NO3-这4种离子(不考虑来源于水电离的离子)的溶液,且4种离子的浓度均为1mol/L | |
| C. | HCl、FeCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 | |
| D. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
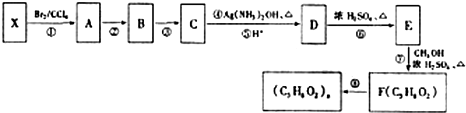
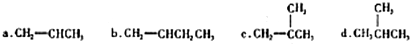
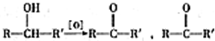 不易被氧化成羧酸
不易被氧化成羧酸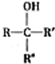 不易被氧化成醛或酮
不易被氧化成醛或酮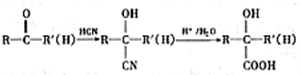
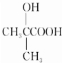 .
.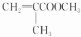 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$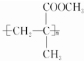 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇汽油推广的最主要的目的在于降低国际市场的油料价格 | |
| B. | 生物柴油燃烧不会产生二氧化碳,是一种清洁能源 | |
| C. | 太阳能是一种清洁安全的不可再生能源 | |
| D. | 纳米金属燃料表面积大,易引发,能量释放快 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体,甲是电解质.根据图示转化关系回答:
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体,甲是电解质.根据图示转化关系回答: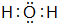 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
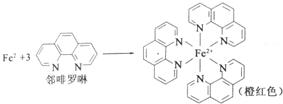
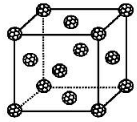
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和H2SO4都属于酸 | B. | K2CO3和K2O都属于盐 | ||
| C. | NaOH和Na2CO3都属于碱 | D. | H2O和O2都属于氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com