
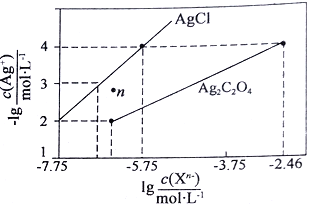
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如下图所示(不考虑C2O42-的水解)。下列叙述正确的是
A.Ksp(Ag2C2O4)的数量级等于10-7
B.n点表示AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4 沉淀
D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为109.04
【答案】D
【解析】
由图形分别求出Ag2C2O4和AgCl的Ksp,利用相关数据进行解题。
A.从图像看出,当c(C2O42-)=10-2.46 mol/L, c(Ag+)=10-4mol/L,Ksp (Ag2C2O4)= 10-2.46×(10-4)2=10-10.46,A错误;
B.根据图像可知c(Ag+)=10-4mol/L,c(Cl-)=10-5.75 mol/L,所以Ksp(AgCl)= 10-4×10-5.75=10-9.75,n点中,c(Ag+)大于平衡时的浓度,Qc(AgCl)> Ksp(AgCl),n点表示AgCl的过饱和溶液,B错误;
C.AgCl中c(Ag+)= Ksp(AgCl)/c(Cl-)=10-9.75/ c(Cl-), Ag2C2O4中
![]() ,假设c(Cl-)=c(C2O42-)=1mol,则Ag2C2O4中c(Ag+)较大,所以向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成AgCl沉淀,C错误;
,假设c(Cl-)=c(C2O42-)=1mol,则Ag2C2O4中c(Ag+)较大,所以向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成AgCl沉淀,C错误;
D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为c(C2O42-)/ c2(Cl-)= c(C2O42-)×c2(Ag+)/ c2(Cl-)×c2(Ag+)=10-10.46/(10-9.75)2=109.04,D正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】我国科学家在太阳能可规模化分解水制氢方面取得新进展——率先提出并验证了一种全新的基于粉末纳米颗粒光催化剂太阳能分解水制氢的“氢农场”策略,其太阳能光催化全分解水制氢的效率创国际最高记录(示意图如图所示,M1、M2 为含铁元素的离子)。下列说法正确的是
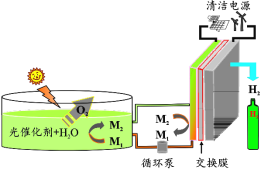
A.制 O2 装置中,太阳能转化为电能
B.制 H2 装置中,交换膜为阴离子交换膜
C.系统制得1mol H2的同时可制得 1mol O2
D.制H2时阳极可发生反应:[Fe(CN)6]4––e- = [Fe(CN)6]3–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F为某增香剂前驱体,其合成路线如图所示(部分反应条件已略去):
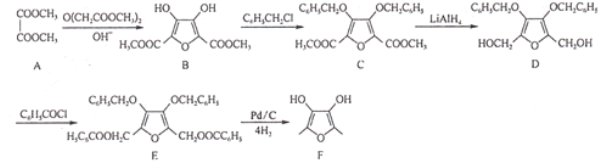
回答下列问题:
(1)A的化学名称为________。
(2)B中除羟基外,其他含氧官能团的名称为________,确定是否存在这些官能团,常用的检测手段是________(填字母)。
a.核磁共振氢谱法b.质谱法
c.红外光谱法d.X一射线衍射法
(3)由B生成C的反应类型为________,设置该步骤的目的是________。
(4)写出由D生成E的化学方程式:________。
(5)写出一种同时满足下列四个条件的B的同分异构体的结构简式:________。
a.属于芳香族化合物,不存在“—O—O—”结构;
b.lmol该物质最多消耗5molNaOH,且与足量的NaHCO3溶液反应最多可生成22.4LCO2(标准状况),
c.核磁共振氢谱显示有4种不同化学环境的氢.
(6)参照上述合成路线,写出以![]() 为原料制备
为原料制备![]() 的合成路线:________。(无机试剂任选)。
的合成路线:________。(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像中的曲线(纵坐标为沉淀或气体的量,横坐标为加入物质的量),其中错误的是
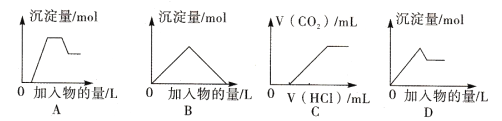
A. 图A表示向含H+、Mg2+、Al3+、NH4+的溶液中滴加NaOH溶液产生沉淀量的关系曲线
B. 图B表示向澄清石灰水中通入二氧化碳直至过量产生沉淀量的关系曲线
C. 图C表示向NaOH和Na2CO3的混合液中滴加盐酸产生CO2气体的关系曲线
D. 图D表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀量的关系曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为不同温度下水的电离平衡曲线,已知pOH=lgc(OH),下列说法正确的是
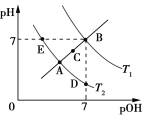
A. T1和T2的关系是:T1>T2
B. KW的关系是:B>C>A=D=E
C. A点到D点:加入少量酸可实现
D. T2时:pH=2的硫酸与pH=12的NaOH溶液等体积混合,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在化工生成等领城应用广泛。
(1)工业尾气中的SO2一直是环境污染的主要原因之一,工业上常采用如下方法降低尾气中的含硫量:
①方法 1: 燃煤中加入生石灰,将SO2转化为 CaSO3,再氧化为CaSO4。
已知:a. CaO(s) +CO2 (g)=CaCO3 △H=-1 78.3kJmol-1
b. 2CaCO3(s) +2SO2(g) +O2(g)=2CaSO4(s) +2CO2(g) △H=-2762.2kJmol-1
c.2 CaSO3(s) + O2(g)=2CaSO4(s) △H =-2314.8 kJmol-1
写出CaO(s)与SO2(g)反应生成CaSO3(s)的热化学方程式:_____________。
②方法 2:用氨水将SO2转化为NH4HSO3 ,再氧化为(NH4)2SO4。实验测得NH4HSO3溶液中![]() = 1500 ,则溶液的pH 为_____________(已知:HSO3-的Ka1=1.5×l0-2, Ka2=l.0×l0-7)。
= 1500 ,则溶液的pH 为_____________(已知:HSO3-的Ka1=1.5×l0-2, Ka2=l.0×l0-7)。
(2)煤制得的化工原料气中含有羰基硫(O=C =S),该物质可转化为H2S,反应为COS(g)+ H2( g ) ![]() H2S(g) +CO(g) △H > 0。
H2S(g) +CO(g) △H > 0。
①恒温恒容条件下,密闭容器中发生上述反应,下列事实不能说明反应达到平衡状态的是________________(填字母)。
a.COS的浓度保持不变 b. 化学平衡常数不再改变
c.混合气体的密度不再改变 d. 形成 2 mol H-S 键的同时形成 1 mol H-H 键
②T℃时 ,在恒容的密闭容器中 ,将定量的CO和H2S 混合加热并达到下列平衡:H2S(g) + CO(g)![]() COS(g) + H2(g),K=0.25,则该温度下反应 COS(g) +H2(g)=H2S(g) +CO(g)的平衡常数K __________。T1℃ 时,向容积为 10 L 的恒容密闭容器中充入 1 molCOS(g)和1 mol H2 (g),达到平衡时 COS 的转化率为_______。
COS(g) + H2(g),K=0.25,则该温度下反应 COS(g) +H2(g)=H2S(g) +CO(g)的平衡常数K __________。T1℃ 时,向容积为 10 L 的恒容密闭容器中充入 1 molCOS(g)和1 mol H2 (g),达到平衡时 COS 的转化率为_______。
(3)过二硫酸(H2S2O8)是一种强氧化性酸,其结构式如图所示: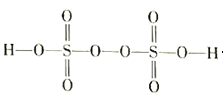
①在Ag+催化作用下,S2O82-能与 Mn2+ 在水溶液中发生反应生成SO42-和 MnO4-,1 molS2O82-能氧化的 Mn2+ 的物质的量为_____________mol。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液制备过二硫酸铵。则阳极的电极反应式为______________________。
(4)NaHS 可用作处理含 Hg2+的污水的沉淀剂,已知 25℃时,反应 Hg2+(aq) + HS-( aq) ![]() HgS(s) + H+(aq) 的平衡常数 K=l.75×l038 ,H2S的电离平衡常数Ka1=1.3×l0-7 , Ka2= 7.0×l 0-15,则Ksp(HgS) =__________________。
HgS(s) + H+(aq) 的平衡常数 K=l.75×l038 ,H2S的电离平衡常数Ka1=1.3×l0-7 , Ka2= 7.0×l 0-15,则Ksp(HgS) =__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温25℃时,下列溶液里微粒间物质的量浓度的关系中正确的是( ):
A. 浓度0.1mol/L的NH4HSO3溶液:c(NH4+)+ c(H+)= c(OH-)+ c(HSO3-)+ c(SO32-)
B. 等体积等浓度Na2S和NaHS混合液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H+)
C. 将0.2mol/LNH3·H2O与0.1mol/LHCl等体积混合:c(Cl-)>c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+)
D. 在0.1mol/L的Na2CO3溶液中:c (OH-)=c(H+)+ c(HCO3-)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们已经学过氢气、氧气、二氧化碳、氯气、二氧化硫、氨气等气体的制备方法和化学性质.以下是实验室制备、洗涤、干燥气体及进行尾气处理的常见仪器装置.请结合所学知识回答下列问题:
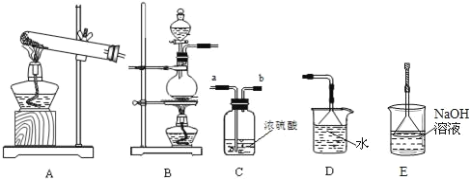
(1)下列气体中,只能用碱石灰干燥的是 ______ (填字母)
A.H2B.Cl2C.SO2D.O2
(2)实验室制取氯气反应原理的离子方程式是______,所选制备装置是______。检验氯气用______试纸;尾气处理的离子方程式为___________。
(3)实验室用氯化铵和熟石灰制取氨气,其化学反应方程式____________。工业上用氯气与石灰乳反应制备漂白粉的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:在300 K时,A(g)+B(g)![]() 2C(g)+D(s)的化学平衡常数K=4,在该温度下,向1L容器中加入1mol A和1mol B发生反应,下列叙述能作为该反应达到平衡状态的标志的是( )
2C(g)+D(s)的化学平衡常数K=4,在该温度下,向1L容器中加入1mol A和1mol B发生反应,下列叙述能作为该反应达到平衡状态的标志的是( )
①C的生成速率与C的消耗速率相等 ②单位时间内生成a mol A,同时消耗2a mol C ③A、B、C的浓度不再变化 ④C的物质的量不再变化 ⑤混合气体的总压强不再变化 ⑥混合气体的密度不再变化
A. ③④B. ①②C. ③⑤D. ④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com