
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
分析 (1)①该反应为熵增大,焓增大的反应,由△G=△H-T△S判断;
②根据达到平衡时的特征“等”、“定”结合反应方程式的特征判断是否达到平衡状态;
(2)反应H2O(g)+CO(g)?H(g)+CO2(g)中,反应物和生成物的体积相等,压强对平衡移动无影响,从等效平衡的角度结合浓度对平衡的影响分析.
解答 解:(1)①该反应为熵增大,焓增大的反应,由△G=△H-T△S,△G<0反应可自发进行,可知该反应在高温时可以自发进行,常温下难以自发进行,故答案为:能;
②Ⅰ由于有固体参加反应,当混合气体的密度不变时,气体的质量不变,说明达到平衡状态;
Ⅱ反应前后气体的体积不等,当容器内气体的压强不变时说明达到平衡状态;
Ⅲ反应前后气体的体积不等,混合气体的总物质的量不变,说明达到平衡状态;
ⅣCO物质的量浓度不变,说明达到平衡状态,则Ⅰ、Ⅱ、Ⅲ和Ⅳ都可说明达到平衡状态,
故答案为:D;
(2)A.丙中浓度最大,甲中浓度最小,浓度越大,反应速率越大,则反应开始时,丙中的反应速率最快,甲中的反应最慢,故A正确;
B. 以甲计算:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始:0 0 0.010 0.010
转化:x x x x
平衡:x x 0.01-x 0.01-x
则$\frac{(0.01-x)×(0.01-x)}{x{\;}^{2}}$=$\frac{4}{9}$,
x=0.006,则平衡时甲中的H2的转化率均是$\frac{0.006}{0.01}$=60%,由于甲和丙的气体的比值相同,为等效平衡状态,则丙中H2的转化率也为60%,故B正确;
C.由B计算可知,平衡时,丙中的c(CO2)是甲中的2倍,应为2×(0.01-0.006)mol/L=0.008mol/L,故C错误;
D.乙与甲相比较,相当于在甲的基础上通入H2,则平衡向逆反应方向移动,平衡时,乙中的CO2的转化率大于60%,故D正确.
故答案为:C.
点评 本题考查化学平衡以及反应热的计算,题目难度较大,本题注意利用三段式法计算,易错点为(2),注意对等效平衡的理解和运用.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ②⑥ | C. | ③④⑤ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0 mol/L | B. | 1.5 mol/L | C. | 1.0 mol/L | D. | 0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2BrCH2Br 二溴乙烷 | B. | CH3CH(NH2)CH2COOH 3-氨基丁酸 | ||
| C. | 硬酯酸甘油脂  | D. | 2,2-二甲基-3-丁醇 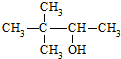 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com