
分析 (1)2、2-二甲基丁烷:该有机物为烷烃,最长碳链含有4个C,两个甲基在2号C,据此写出该有机物的结构简式;
(2)含有C=C双键的碳链有5个碳原子,双键处于端位置,从C=C双键一端编号,甲基处于3、4、4号碳原子上;
(3)3、4-二甲基-3-乙基-已烷,其主链为己烷,最长碳链含有6个C,在3、4号C各含有1个甲基,在3号C含有1个乙基;
(4)2,6-二甲基-4-乙基辛烷,其主链为辛烷,最长碳链含有8个C,在2、6号C各含有1个甲基,在4号C含有1个乙基;
(5)2-氯-丙烷,其主链为丙烷,最长碳链含有3个C,在2号C含有1个氯原子.
解答 解:(1)2、2-二甲基丁烷:主链为丁烷,在2号C含有2个甲基,该有机物的结构简式为:CH3C(CH3)2CH2CH3,
故答案为:CH3C(CH3)2CH2CH3;
(2)依据系统命名方法,结合名称写出结构简式3,4,4-三甲基-1-戊烯的结构简式为:CH2=CHCH(CH3)C(CH3)2CH3,
故答案为:CH2=CHCH(CH3)C(CH3)2CH3;
(3)3、4-二甲基-3-乙基-已烷,其主链为己烷,最长碳链含有6个C,在3、4号C各含有1个甲基,在3号C含有1个乙基,该有机物的结构简式为:CH3CH2C(C2H5)(CH3)CH(CH3)CH2CH3,
故答案为:CH3CH2C(C2H5)(CH3)CH(CH3)CH2CH3;
(4)2,6-二甲基-4-乙基辛烷,其主链为辛烷,最长碳链含有8个C,在2、6号C各含有1个甲基,在4号C含有1个乙基,该有机物的结构简式为:CH3CH(CH3)CH2CH(C2H5)CH2CH(CH3)CH2CH3,
故答案为:CH3CH(CH3)CH2CH(C2H5)CH2CH(CH3)CH2CH3;
(5)2-氯-丙烷,其主链为丙烷,最长碳链含有3个C,在2号C含有1个氯原子,该有机物的结构简式为:CH3CH(Cl)CH3,
故答案为:CH3CH(Cl)CH3.
点评 本题考查了有机物的命名、结构简式的书写,题目难度不大,试题侧重了基础知识的考查,注意掌握常见有机物的命名原则,能够根据名称书写有机物的结构简式.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙酸的结构简式:C2H4O2 | B. | Cl-的结构示意图为 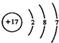 | ||
| C. | 中子数为20 的氯原子:3717Cl | D. | NH3 的电子式: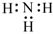 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | SiO2等不溶于酸的物质 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |

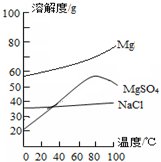
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡常数的大小只与温度有关,而与浓度、压强、催化剂等无关 | |
| B. | 在任何条件下,化学平衡常数都是一个定值 | |
| C. | 在平衡常数表达式中,反应物浓度用起始浓度,生成物浓度用平衡浓度 | |
| D. | 从平衡常数大小可以推断一个反应进行的快慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述过程中,由1 mol CuFeS2制取1 mol Cu时共消耗2 mol O2 | |
| B. | 冶炼过程中的尾气可用来制硫酸 | |
| C. | 在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 | |
| D. | 电解精炼铜的过程中,每转移1 mol电子时,阳极溶解铜的质量为32 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入KSCN溶液,出现红色,一定不含Fe2+ | |
| B. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| C. | SiO2与Al2O3都既可以与酸又可以与碱反应,故都是两性氧化物 | |
| D. | 玻璃、水泥、陶瓷、刚玉都是硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 实验目的 | T/K | pH | c/10-3 mol/L | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 313 | 3 | 6.0 | 0.30 |
| ③ | 探究溶液的pH对降解反应速率的影响 | 298 | 10 | 6.0 | 0.30 |
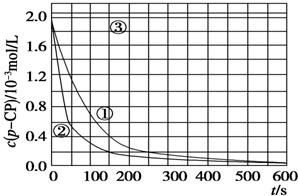 [数据处理]
[数据处理]查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com