
【题目】氰化钠(NaCN)是一种重要的化工原料、有剧毒,一旦泄露可以通过喷洒双氧水或硫代硫酸钠溶液来处理。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为___________;用硫代硫酸钠处理1mol NaCN时,反应中转移电子的物质的量为 。
(2) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是 。
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:
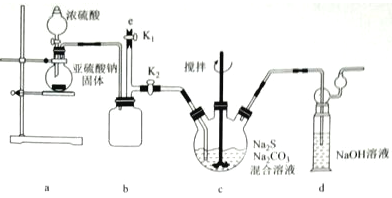
b装置的作用是___________;c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有_____________。
实验结束后,在e处最好连接盛____________(填化学式)的注射器,再关闭K2打开K1,以防拆除装置过程中的有害气体污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用_________(填仪器名称)盛装;滴定终点时的现象是___________。
处理后的废水是否达到排放标准:__________(填“是”或“否”),其依据是__________(用实验数据说明)。
【答案】+2;1mol;CN-+H2O2+H2O=HCO3-+NH3↑(2分)
(3)①安全瓶,防止倒吸;Na2SO3、Na2SO4;
②NaOH溶液;③酸式滴定管;出现浅(黄)色沉淀,且半分钟内不消失
④否;消耗AgNO3的物质的量为:2.5×10-3L×0.0001mol/L=2.50×10-7mol,根据方程式Ag++2CN-=[Ag(CN)2]-,处理的废水中氰化钠的质量为2.50×10-7mol×2×49g/mol=2.45×10-5g,废水中氰化钠的含量为:0.98mg/L,不达标。(答出氰化钠的含量0.98mg/L即可给分)
【解析】
试题解析:(1)根据化合价法则:Na 为+1价;N为-3价,C为+2价;根据反应NaCN+Na2S2O3==NaSCN+Na2SO3;Na2S2O3中+2价硫降低到NaSCN中0价硫;升高到Na2SO3中+4价硫;处理1mol NaCN时,反应中转移电子的物质的量为1摩尔;(2) NaCN用双氧水处理后,产生一种酸式盐碳酸氢钠和一种能使湿润红色石蕊试纸变蓝的气体氨气,CN-+H2O2+H2O=HCO3-+NH3↑;(3)①安全瓶,防止倒吸;二氧化硫气体如果过量,进入d装置中的氢氧化钠中,还可能含有的溶质:亚硫酸钠、硫酸钠等;②在b中会有二氧化硫气体剩余,应该用氢氧化钠溶液吸收;③AgNO3溶液水解显酸性,应用酸式滴定管盛装;由于AgI呈黄色,且CN-优先于Ag+反应。氰化钠与AgNO3溶液反应结束后,碘离子与银离子作用生成黄色沉淀;答案为出现浅(黄)色沉淀,且半分钟内不消失;④消耗AgNO3的物质的量为:2.5×10-3L×0.0001mol/L=2.50×10-7mol,根据方程式Ag++2CN-=[Ag(CN)2]-,处理的废水中氰化钠的质量为2.50×10-7mol×2×49g/mol=2.45×10-5g,废水中氰化钠的含量为:0.98mg/L,不达标。


科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )

A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下,则下列判断正确的是( )
![]()
A.MFe2Ox是氧化剂
B.SO2是该反应的催化剂
C.x<y
D.MFe2Oy是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某些化学知识用数轴表示,可以收到直观、简明、易记的效果。用数轴表示的下列知识正确的是( )
A.硫及其化合物的化合价与氧化还原反应的关系:

B.分散系的分类:

C.AlCl3溶液与NaOH溶液反应后铝元素的存在形式:

D.CO2与NaOH溶液反应后的产物

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第二次世界大战期间丹麦科学家玻尔被迫离开德军占领的祖国.为了表明一定要返回祖国的决心,他把心爱的金质诺贝尔奖章放在盛有“王水”(浓盐酸和浓硝酸的混合物)的玻璃容器中:Au+HNO3+3HCl═AuCl3+NO↑+2H2O.战后玻尔返回祖国,从溶液中提取出金,又重新铸造成奖章.下列方法中,不能从溶有金的王水中提取出金的是( )
A.萃取
B.蒸发灼烧
C.用Fe置换
D.电解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成。某兴趣小组以两种途径分别对X进行如下实验探究。

下列有关说法不正确的是( )
A.无法判断混合物中是否含有Na2O
B.由II可知X中一定存在SiO2
C.1.92g 固体成分为Cu
D.15.6g混合物X中m(Fe2O3):m(Cu)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.液溴易挥发,在存放液溴的试剂瓶中应加水封
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关AgCl沉淀的溶解平衡的说法中正确的是( )
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.在有AgCl沉淀生成的溶液中加入NaCl固体,AgCl沉淀溶解的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
A.在常温常压下为液体
B.能使酸性KMnO4溶液褪色
C.可自身加成形成聚乙烯
D.能使溴的CCl4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com