
分析 (1)向氨水中加入氯化镁固体时,镁离子和氢氧根离子反应生成氢氧化镁沉淀,促进一水合氨电离;
(2)向氨水中加入浓盐酸时,氢离子会消耗氢氧根离子,氢氧根离子浓度减小,促进一水合氨电离;
(3)向浓氨水中加入少量NaOH固体,导致溶液中氢氧根离子浓度增大,平衡向左移动.
解答 解:①向氨水中加入氯化镁固体时,镁离子和氢氧根离子反应生成氢氧化镁沉淀,氢氧根离子浓度减小,促进一水合氨电离,则溶液中铵根离子浓度增大,
故答案为:右;减小;增大;
(2)向氨水中加入浓盐酸时,氢离子会消耗氢氧根离子,氢氧根离子浓度减小,一水合氨的电离平衡向右移动,NH3、NH3•H2O的浓度均减小,
故答案为:OH-、NH3、NH3•H2O;
(3)向浓氨水中加入少量NaOH固体,导致溶液中氢氧根离子浓度增大,平衡向左移动,氢氧根离子和铵根离子反应生成氨气,所以有刺激性气体逸出,
故答案为:左;有刺激性气体逸出.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,再结合溶液中离子浓度变化确定平衡移动方向,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

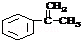 .
.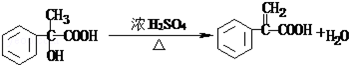 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{2}^{4}$He原子核内含有4个质子 | B. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | ||
| C. | ${\;}_{2}^{3}$He原子核内含有3 个中子 | D. | ${\;}_{2}^{4}$He具有较强的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人体缺乏维生素C会引起夜盲症 | |
| B. | 可用肥皂水区别硬水与软水 | |
| C. | 在化学反应中只有燃烧才能放出热量 | |
| D. | 合成橡胶、合金都属于合成材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
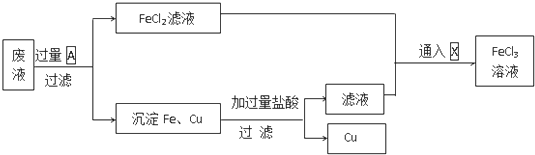
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | B. | Fe+H2SO4═FeSO4+H2↑ | ||
| C. | 3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | D. | 4NH3+3O2$\frac{\underline{\;高温\;}}{\;}$2N2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的AlCl3溶液中含有Al3+离子数为0.1NA | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 在密闭容器中加入1.5mol H2和0.5mol N2充分反应后可得到NH3为1NA | |
| D. | 常温下16g O2与O3的混合气体中含氧原子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com