
| A、Pb 为正极被氧化 |
| B、溶液的pH不断减小 |
| C、放电时负极反应式是PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| D、溶液pH不断增大 |


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a=b | B、a<b |
| C、a>b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NH4+、Br-、Cl- |
| B、K+、Na+、SO42 -、SiO32 - |
| C、Na+、HCO3-、SO32 -、CH3COO- |
| D、H+、Fe3+、NO3-、SO32 - |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、HCO3-、Cl- |
| B、K+、Br-、AlO2-、Cl- |
| C、SO42-、Na+、NO3-、Cl- |
| D、SO42-、NH4+、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
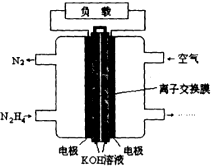 肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.
肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠溶液中加入CaCl2溶液产生白色沉淀物 |
| B、硫酸铜溶液中插入铁片,铁片上出现红色沉淀物 |
| C、向双氧水中加入二氧化锰产生气泡 |
| D、铁在氧气中燃烧,剧烈反应火星四射 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序:X>Y>Z |
| B、Z单质与X单质直接反应可生成两种化合物 |
| C、工业上,电解X和Y形成的化合物制取Y单质 |
| D、Y、Z元素的最高价氧化物对应的水化物不能互相反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| B、向Ca(ClO)2溶液中通入适量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C、向FeBr2溶液中加少量氯水:2Fe2++Cl2=2Fe3++2Cl- |
| D、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com