
| A. | 2Na+2H2O=2NaOH+H2↑是酸碱反应 | |
| B. | ClO-+H2O?HClO+OH-是酸碱反应 | |
| C. | 碱性强弱顺序:OH->ClO->CH3COO- | |
| D. | HCO3-既是酸又是碱,NH3既不是酸又不是碱 |
分析 酸碱质子理论:凡是能够给出质子(H+)的物质都是酸、凡是能够接受质子的物质都是碱,所以所有酸都能够释放出H+,能结合H+的都是碱.为酸碱两性物质的是属于酸又属于碱,必须符合能给出质子又能结合质子,据此即可解答.
解答 A、活泼金属与水发生的氧化还原反应,而不是酸碱反应,故A错误;
B、C1O-接受质子是碱,而H2O给出质子是酸,所以C1O-+H2O?HClO+OH-是酸碱反应,故B正确;
C、物质碱性的强弱取决于分子或离子接受质子能力的大小,氢氧根接受质子能力强次氯酸根离子,次氯酸根强于醋酸根离子,故C正确;
D、NH3可以结合质子是碱,HCO3-既可以给出质子也可以接受质子,所以既是酸又是碱,故D错误;
故选BC.
点评 本题考查两性物质的概念,解答本题关键是要严格按照酸与碱的定义考虑,是能给出质子(H+)还是能接受质子,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ④⑤ | C. | ④⑥ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 移液时,不慎将液体流到瓶外 | |
| B. | 容量瓶中原有少量的蒸馏水 | |
| C. | 容量瓶盛过Na2CO3溶液,使用前未洗涤 | |
| D. | 定容时读数仰视 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定溶液的酸碱度时,先将pH试纸用水润湿,后沾上被测溶液 | |
| B. | 点燃可燃性气体如H2、CO等时,先检验气体纯度后点燃 | |
| C. | 实验室稀释浓硫酸时,可以在量筒中进行 | |
| D. | 试管和烧杯都可以直接用火焰加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①② | C. | ② | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾具有消毒杀菌作用,可用于净水 | |
| B. | BaSO4在医学上用做钡餐,Ba2+对人体无毒 | |
| C. | 氢氧化铝常用于治疗胃酸过多 | |
| D. | 用催化法处理汽车尾气中的CO和NO:CO+NO$\stackrel{催化剂}{→}$C+NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积减半,则压强为原来的两倍 | |
| B. | 平衡向右移动,混合气体的颜色一定会变浅 | |
| C. | 平衡向右移动,混合气体的密度不变 | |
| D. | 体积减半,压强增大,但小于原来的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
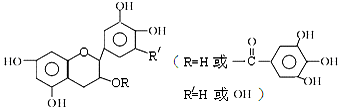
| A. | 儿茶素能与FeCl3溶液发生显色反应 | |
| B. | 1mol儿茶素最多可与10mol NaOH反应 | |
| C. | 常温下,儿茶素不溶于水,也不溶于有机溶剂 | |
| D. | 儿茶素一定不能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com