
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | |
| B. | M和T形成的化合物既能与强酸反应又能与强碱反应 | |
| C. | 单质与等浓度的稀盐酸反应的剧烈程度为Q>L | |
| D. | L2+与R2-的核外电子数相等 |
分析 短周期元素,由元素的化合价可知,T、R都有-2价,而R有+6价且原子半径较大,则T为O元素,R为S元素,L、Q均有+2价,处于ⅡA族,原子半径L>Q,则L为Mg、Q为Be,M只有+3价,处于ⅢA族,原子半径大于硫,则M为Al元素.
A.水分子之间存在氢键,沸点高于硫化氢;
B.氧化铝能与酸反应生成相应的盐与水,与碱反应生成相应的盐与水;
C.金属性越强,与酸反应越剧烈;
D.核外电子数=质子数-离子带的电荷.
解答 解:短周期元素,由元素的化合价可知,T、R都有-2价,而R有+6价且原子半径较大,则T为O元素,R为S元素,L、Q均有+2价,处于ⅡA族,原子半径L>Q,则L为Mg、Q为Be,M只有+3价,处于ⅢA族,原子半径大于硫,则M为Al元素.
A.水分子之间存在氢键,硫化氢分子之间为范德华力,氢键比较范德华力强,故沸点H2O>H2S,故A错误;
B.M与T形成的化合物是氧化铝,是两性氧化物,故B正确;
C.金属性Mg比Be强,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为L>Q,故C错误;
D.L2+的核外电子数为12-2=10,R2-的核外电子数为16-(-2)=18,不相等,故D错误.
故选B.
点评 本题考查结构性质位置关系应用,利用原子半径及化合价来推断出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质来解答即可,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
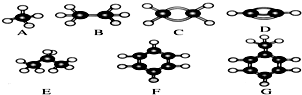
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
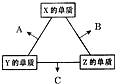 X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16.在适当条件下三种单质两两化合,可发生如图所示变化.己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个.请回答下列问题:由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为HNO3、NH4NO3、NH3.H2O.
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16.在适当条件下三种单质两两化合,可发生如图所示变化.己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个.请回答下列问题:由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为HNO3、NH4NO3、NH3.H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水 | B. | 干冰受热直接变成气体 | ||
| C. | HCl溶解于水 | D. | 打雷放电时,O2变成O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

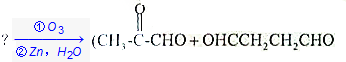

 .
. +(m-1)H2O.②B-C、C-E的反应类型分别为:加成反应、缩聚反应.
+(m-1)H2O.②B-C、C-E的反应类型分别为:加成反应、缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
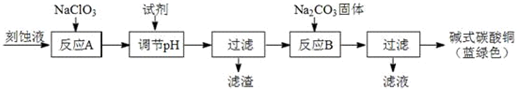
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到平衡时,Ⅰ途径的反应速率V(A)等于Ⅱ途径的反应速率V(A) | |
| B. | 达到平衡时,第Ⅰ条途径混合气体的密度与第Ⅱ条途径混合气体的密度相同 | |
| C. | Ⅰ和Ⅱ两途径最终达到平衡时,体系内混合气体的体积分数相同 | |
| D. | Ⅰ和Ⅱ两途径最终达到平衡时,体系内混合气体的体积分数不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com