
【题目】I. 恒温、恒压下,在一个可变容积的容器中发生如下反应:A(g)+B(g)![]() C(g)
C(g)
(1)若开始时放入1mol A和1mol B,到达平衡后,生成amol C。这时A的物质的量为_____mol。
(2)若开始时放入3mol A和3mol B,到达平衡后,生成C的物质的量为____mol。
(3)若开始时放入xmol A、2mol B和1mol C,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=___mol,y=___mol。平衡时,B的物质的量________(选填一个编号)。
(甲)大于2mol (乙)等于2mol (丙)小于2mol (丁)可能大于、等于或小于2mol
II. 若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(4)开始时放入1mol A和1mol B到达平衡后生成bmol C,将b与(1)小题的a进行比较,则________(选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
【答案】(1)1-a (2)3a (3)2 3-3a 丁 (4)a/(2-a) (5)乙
【解析】
(1)生成a mol C,则根据方程式可知,消耗A是amol,所以平衡时A是(1-a)mol。
(2)由于是等温等压,所以平衡是等效的,因此平衡时生成C的物质的量为3amol。
(3)因为平衡时C的物质的量是3amol,所以AB的起始量应该是3mol和3mol。1molC相当于1molA和1molB,所以x=2mol,平衡时A的物质的量是(3-3a)mol;由于最初反应进行的方向是不能确定的,所以平衡时B的物质的量可能是大于2mol或小于2mol或等于2mol,答案选丁。
(4)若在(3)的平衡混合物中再加入3molC,则平衡还是等效的,所以其质量分数是
![]()
(5)因为反应是体积减小的可逆反应,所以在恒压的条件下,反应物的转化率高,因此a大于b,答案选乙。


科目:高中化学 来源: 题型:
【题目】为测定某烃A的分子组成和结构,对这种烃进行以下实验:①取一定量的该烃,使其完全燃烧后的气体通过装有足量无水氯化钙的干燥管,干燥管增重7.2g;再通过足量石灰水,石灰水增重17.6g。②经测定,该烃(气体)在标准状况下的密度为1.25g·L-1。
I.现以A为主要原料合成某种具有水果香味的有机物,其合成路线如图所示。

(1)A分子中官能团的名称是______,E的结构简式为________。
(2)写出以下反应的化学方程式,并标明反应类型。反应③的化学方程式是__________; G是生活中常见的高分子材料,合成G的化学方程式是________________________;
Ⅱ.某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
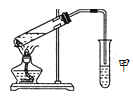
(1)实验开始时,试管甲中的导管不伸入液面下的原因是_______________;当观察到试管甲中________ 现象时认为反应基本完成。
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。
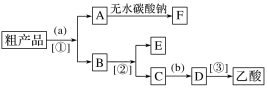
试剂b是____________;分离方法①是__________;分离方法③是________。
(3)在得到的A中加入无水碳酸钠粉末,振荡,目的是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分子、原子、离子的说法,错误的是( )
①二氧化碳由碳原子和氧原子构成;②等质量的氧气和液氧,氧气体积比液氧大,说明分子间隙发生了改变;③分子是保持物质性质的一种微粒;④分子一定比原子大;⑤原子是最小的粒子,不可再分
A.①③④⑤B.②③④⑤
C.①②③④⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.18O2和16O2互为同位素
B.正己烷和2,2二甲基丙烷互为同系物
C.C60和C70是具有相同质子数的不同核素
D.迄今为止人们发现了118种元素,即有118种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律.
Ⅰ.甲同学设计了如下图装置来一次性完成元素氮、碳、硅非金属性强弱的比较。
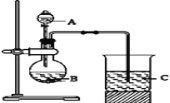
(1)甲同学在连接好仪器后,加入药品之前要检查装置气密性。首先关闭_____,将导管伸入烧杯液面以下,再_____,如果C中______,则说明________
(2)要证明氮、碳、硅非金属性强弱,在A中加________溶液,B中加____溶液,C中加________溶液,将观察到C中__________的现象.但老师认为,该现象不足以证明三者非金属性强弱,请用文字叙述理由_______。
(3)为避免上述问题,应在B、C之间增加一个盛有足量____(选填下列字母:A.浓盐酸 B.浓NaOH溶液C.饱和Na2CO3溶液 D.饱和NaHCO3溶液)的洗气装置.改进后C中发生反应的离子方程式是__________ .
Ⅱ.丙同学设计了如下图装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润淀粉KI试纸、湿润红纸.
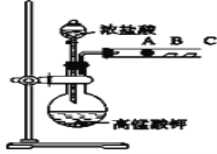
(1)请写出浓盐酸与高锰酸钾反应的离子方程式_________________
(2)A中棉花颜色变_______,则说明非金属性Cl>Br;向NaBr和KI的混合溶液中,通入足量的Cl2充分反应后,将所得溶液蒸干并灼烧,最后得到的物质是_________
(3)丙同学利用此实验证明卤素单质氧化性:Cl2>Br2>I2,你认为合理吗____,(填“合理”或“不合理”)理由是___________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用以下装置探究氯气和氨气之间的反应情况。其中A、F分别为氨气和氯气的制取发生装置,C为纯净干燥的氯气与干燥的氨气发生反应的装置。请回答下列问题:

(1)实验室通常用来制取氨气的化学方程式为 ________________________;
(2)实验室收集制备得到的氨气的常用方法是______________________。
(3)请为B处虚线框内选择可能合适的装置以及相应的试剂名称______填序号。
A.球形干燥管装碱石灰 B.洗气瓶装浓硫酸
C.球形干燥管装氧化钙 D.球形干燥管装氢氧化钠
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一请写出反应的化学方程式: __________________若有1molNH3被氧化,则转移的电子数目为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com