
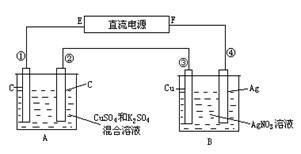
如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL。
⑴电源F为____________极;第②极为__________极; B池为___________池;
⑵A池中第②极上的电极反应式为__________________ ___;
A池中第①极上产生气体体积为__________________ mL;(标准状况下)
(3) 通电前A池中原混合溶液Cu2+的浓度为 ;
(1) 正 阳 电解(镀)池
(2)4OH- - 4 e- = 2H2O+O2 zxxk
(3)112ml 0.025 mol·L-1
【解析】(1)第③极增重2.16 g,说明该电极是阴极,则银电极是阳极,所以F是正极,E是负极,①②分别就是阴极和阳极。铜电极上的电极反应式为Ag++e-=Ag,反应中转移电子的物质的量为 。
。
(2)惰性电极电解硫酸铜和硫酸钾的混合液时阳极失去电子,即溶液中的OH-被氧化生成氧气,反应式是4OH- - 4 e- = 2H2O+O2↑。根据得失电子守恒可知氧气的物质的量是 ,其体积是
,其体积是 。
。
(3)由(1)、(2)分析可知在A池中阴极上也有气体生成,其体积是112ml,这说明硫酸铜不足,当铜离子放电之后,溶液中的氢离子放电,根据电荷守恒可知析出的铜是0.005mol,所以通电前A池中原混合溶液Cu2+的浓度为 。
。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)
目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)| 电极 | a | b | c | d | e | f |
| 石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
| 溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
C(s)+O2(g)![]() CO2(g) ΔH2=-393.5 kJ·mol-1
CO2(g) ΔH2=-393.5 kJ·mol-1
则298 K时CO(g)在O2(g)燃烧生成CO2(g)的热化学反应方程式为_____________________;
(2)一种新型的熔融盐燃料电池具有高发电效率而备受重视。现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通入CO气体,另一极通入空气与CO2的混合气体,制得燃料电池。
该电池工作时的负极反应式为______________________________;
熔融盐中![]() 的物质的量在工作时______________(填“增大”“减小”“不变”)。
的物质的量在工作时______________(填“增大”“减小”“不变”)。
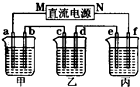
Ⅱ.如下图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液见图。

(1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源a端为_________极,通电一段时间后,观察到滤纸d端出现的现象是________________;

(2)已知C装置中溶液为Cu(NO3)2和X(NO3)3,且均为0.1 mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示。则Cu2+、X3+、H+氧化能力由大到小的顺序是___________;D装置Cu极的电极反应式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)如图所示3套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0、2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0、5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0、64 g。
① 电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
② 乙烧杯中电解反应的离子方程式为 ;
③ 甲、乙两烧杯中生成的气体标准状况下共 mL。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江临海市白云高级中学高二下学期期中考试化学卷(带解析) 题型:实验题
(每空1分,共7分)如图所示3套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量,电极增重 0.64 g。
①电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
②乙烧杯中电解反应的离子方程式为 ;
③甲、乙两烧杯中生成的气体标准状况下共 mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com