
|
��һ�ݻ�Ϊ1 L���ܱ������м���һ������X��Y��������ѧ��ӦaX(g)��2Y(s)
| |
A�� |
��X��ʾ0��10 min�ڸ÷�Ӧ��ƽ������Ϊ0.025 mol/(L��min) |
B�� |
������ͼ����÷���ʽ��a��b��2��1 |
C�� |
0��10 min�����������ѹǿ������ |
D�� |
��13 minʱ���߱仯��ԭ�������������Z���� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ���ӱ�ʡ������ѧ2011�������ѧ�ڵ��Ĵ��¿���ѧ���� ���ͣ�013
|
��һ�ݻ�Ϊ1 L���ܱ������м���һ������X��Y��������ѧ��ӦaX(g)��2Y(s)
| |
| [����] | |
A�� |
��X��ʾ0��10 min�ڸ÷�Ӧ��ƽ������Ϊ0.025 mol/(L��min) |
B�� |
������ͼ����÷���ʽ��a��b��2��1 |
C�� |
0��10 min�����������ѹǿ����С |
D�� |
��13 minʱ���߱仯��ԭ�������������Z���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������ѧ2011��2012ѧ��߶���ѧ�����п��Ի�ѧ���� ���ͣ�022
��һ�ݻ�Ϊ1 L���ܱ������м���һ������X��Y��������ѧ��ӦX(g)��2Y(s)![]() 2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߣ�
2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߣ�
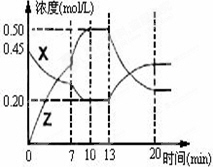
(1)0��10 min�����������ѹǿ��________��(��������С������ȷ����)
(2)�Ʋ��ڵ�7 minʱ���߱仯��ԭ�������________��13 minʱ���߱仯��ԭ�������________(�����)
������Z����
������X����
������
�ܽ���
��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ����һ��2011��2012ѧ��߶���ѧ�����п��Ի�ѧ���� ���ͣ�022
����1 L������ͨ��CO2��H2��2 mol����һ�������·�����Ӧ��CO2��H2![]() CO��H2O���ش��������⣺
CO��H2O���ش��������⣺
(1)��830�������£���Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50�������������ƽ�ⳣ��K1��________��
(2)��(1)�Ļ����ϣ�����ϵ�¶Ƚ���800�森��֪�������µ�ƽ�ⳣ��K2��0.81��������֪�÷�Ӧ������ӦΪ________��Ӧ(����ȡ��������ȡ�)��
(3)��(1)�Ļ����ϣ�ѹ���������֮0.5 L���������µ�ƽ�ⳣ��ΪK3����K3________K1
(4)T��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n(CO2)��1.2 mol��n(H2)��1.5 mol��
n(CO)��0.9 mol��n(H2O)��0.9 mol�����ʱ�÷�Ӧ________���У�(�������Ӧ�������淴Ӧ������ƽ��״̬��)��
����һ�ݻ�Ϊ1 L���ܱ������м���һ������X��Y��������ѧ��ӦX(g)��2Y( s)![]() 2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߣ�
2Z(g)����H��0����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߣ�
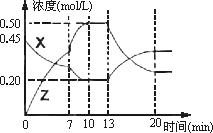
(1)0��10 min�����������ѹǿ��________��(��������С������ȷ����)
(2)�Ʋ��ڵ�7 minʱ���߱仯��ԭ�������________��13 minʱ���߱仯��ԭ�������________(�����)
������Z����
������X����
������
�ܽ���
��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�긣��ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��Դ�����ö�����̼�����ɼ�������������ŷţ��������»��ȼ�ϻ���Ҫ��ҵ��Ʒ��
��1���п�ѧ�����������FeO���պ�����CO2������Ȼ�ѧ����ʽ���£�6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ��H=-76.0 kJ��molһ1
��������Ӧ��ÿ����1 mol Fe3O4��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
����֪��C(s)+2H2O(g)=CO2(g)+2H2(g) ��H=+113.4 kJ��molһ1����Ӧ��3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)�ġ�H=__________��
��2����һ�������£�������̼ת��Ϊ����ķ�Ӧ���£�CO2(g)+4 H2 (g)  C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2
0.2 mol��Lһ1��H2
0.8 mol��Lһ1��CH40.8
mol��Lһ1��H2O1.6
mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��
C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2
0.2 mol��Lһ1��H2
0.8 mol��Lһ1��CH40.8
mol��Lһ1��H2O1.6
mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��
��3����ʢ�ٴ�ѧ���о���Ա�о���һ�ַ�������ʵ��ˮ������ʱCO2���ŷţ������ԭ����
ͼ��ʾ:

�������������̵�����ת����ʽ��____________________��
��������ⷴӦ���¶�С��900��ʱ���У�̼����ȷֽ�ΪCaO��CO2�������Ϊ����̼���ƣ��������ĵ缫��ӦʽΪ___________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com