
ʵ��������500mL0.2mol•L��1��FeSO4��Һ�������������Ϊ��
������ƽ�ϳ�ȡһ���������̷���FeSO4•7H2O�������������ձ��У�������������ˮʹ����ȫ�ܽ⣻
�ڰ��Ƶõ���ҺС�ĵ�ע��500mL������ƿ�У�
�ۼ���������ƿ�еμ�����ˮ��Һ���̶���1��2cm��ʱ�����ý�ͷ�ι�С�ĵμӣ�ֱ����Һ�İ�Һ��ǡ����̶�������Ϊֹ��
������������ˮϴ���ձ��Ͳ�����2��3�Σ�ÿ�ε�ϴ��Һ��ת������ƿ�У�������ҡ�ȣ�
�ݽ�����ƿ���ã����ҡ�ȡ�
����д���пհף�
��1����������ƽ��ȡ���̷�������Ϊ�� ��
��2��������������ȷ˳��Ϊ�� ��
��3������ʵ������ж���õ������������ܽ�ʱ�������������ǣ� ������Һʱ�������������ǣ� ��
��4���۲�Һ��ʱ�������ӿ̶��ߣ���ʹ�����Ƶ���Һ��Ũ�� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족��ͬ����������ˮʱ���������˿̶��ߺ�������Һ��ʹҺ����̶������У��� ��
��5���æ�=1.84g•mL��1����������Ϊ98%��Ũ��������200mL1mol•L��1��ϡ����������������Һ�IJ����ϵIJ����Ҫ�����㣺
�ټ��㣺������ӦȡŨ��������V= mL����ȷ��С�������λ����
����ȡ��������Ͳ��һ�ִ��Ե����ߣ����뾫ȷ��ȡ������ѡ�� �����������ƣ���
���ܡ�������
ϡ��Ũ����ķ��� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ̩���н������߶���ѧ������ѡ��ѧ�Ծ��������棩 ���ͣ������
�״�������Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϡ����úϳ���(��Ҫ�ɷ�ΪCO��CO2��H2)�ڴ����������ºϳɼ״�������������Ӧ���£�
��CO(g)��2H2(g) 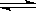 CH3OH(g) ��H1=��99 kJ��mol��1
CH3OH(g) ��H1=��99 kJ��mol��1
��CO2(g)��3H2(g) 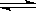 CH3OH(g)��H2O(g) ��H2=��58 kJ��mol��1
CH3OH(g)��H2O(g) ��H2=��58 kJ��mol��1
��CO2(g)��H2(g) 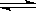 CO(g)��H2O(g) ��H3=��41 kJ��mol��1
CO(g)��H2O(g) ��H3=��41 kJ��mol��1
�ش��������⣺
��1����Ӧ�ٵĻ�ѧƽ�ⳣ��K�ı���ʽΪ ����ͼ������ȷ��ӳ�÷�Ӧƽ�ⳣ��K���¶ȱ仯��ϵ������Ϊ (�a����b��)�����ж������� ��

��2���ϳ��������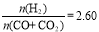 ʱ����ϵ�е�COƽ��ת����(a)���¶����߶���С����������Ҫԭ���У���Ӧ��Ϊ���ȷ�Ӧ��ƽ�������ƶ���ʹ����ϵ��CO���������� ��
ʱ����ϵ�е�COƽ��ת����(a)���¶����߶���С����������Ҫԭ���У���Ӧ��Ϊ���ȷ�Ӧ��ƽ�������ƶ���ʹ����ϵ��CO���������� ��
��3������һ�������£��ݻ��㶨ΪVL�ķ�Ӧ���г���amolCO��2amolH2���ڴ��������½�������Ӧ�٣����д�ʩһ��ʹc(CH3OH)/c(CO)������� ������ĸ����
A�������¶� B������Ar(g)ʹ��ϵ����ѹ����
C�����º����ٳ���H2 D�����º����ٳ���a mol CO��2a mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ɹų���������ظ�����ѧ�ڵ�һ��ͳ����ѧ�Ծ��������棩 ���ͣ��ƶ���
��֪��A��B��C��D��E��F����Ԫ�غ˵�����������������ڱ���ǰ�����ڵ�Ԫ�ء�����Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�CԪ���ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ�������ߣ�F���γɺ�ɫ����ש��ɫ����F2O�ͺ�ɫ��FO���������
�ش��������⣺
��1��F��ԭ�ӵ�M������Ų�ʽΪ ��
��2��B��C��D�ĵ�һ��������С�����˳��Ϊ ������Ԫ�ط��ű�ʾ��
��3��A�ļ��⻯����Ӽ�������ˮ������Ҫԭ���� .
��4��E�������������ӵĿռ乹���� ��������ԭ�ӵ��ӻ���ʽΪ ��
��5��F�ĸ�������A�ļ��⻯���γɵ������ӣ���λ��Ϊ ��
��6��A��F�γ�ij�ֻ�����ľ����ṹ��ͼ��ʾ�����仯ѧʽΪ ������ɫ���ʾFԭ�ӣ�����֪���ڵİ��������֮��ľ���Ϊa cm�� �þ������ܶ�Ϊ g/cm3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ɣ���ݴ�ѧ(ASU)�Ͱ�������ʵ���ҵĿ�ѧ����Ƴ�����������������Ҷ��ԭ��Ϊ��2H2O(g)  2H2(g)��O2(g)���йظ÷�Ӧ��˵����ȷ����
2H2(g)��O2(g)���йظ÷�Ӧ��˵����ȷ����
A����H ��0
B��������H2�� O2�����е����������ڷ�Ӧ��H2O�����е�������
C����ѧ��ת��Ϊ����
D���������������ɫ��Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�߶���ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ������
��֪�Ȼ�ѧ����ʽH��(aq)��OH��(aq)===H2O(l) ��H����57.3kJ/mol��
��1��ʵ������0.25 L 0.10mol/L��һԪǿ���ǿ���кͣ����кͺ���Һ���Ϊ0.5 L���кͺ����Һ�ı�����Ϊ4.2��10��3kJ/(g����)�����ܶ�Ϊ1.0g/mL������Һ�¶�����____________�档
��2����V1mL 1.0mol/L HCl��Һ��V2mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ��������ͼ��ʾ(ʵ����ʼ�ձ���V1��V2��50mL)������������ȷ����( )

A������ʵ��ʱ�����¶�Ϊ22��
B����ʵ�������ѧ�ܿ���ת��Ϊ����
C��NaOH��Һ��Ũ��ԼΪ1.0mol/L
D����ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ
��3��������ˮ��ȡ������Դ�����������о�������ȷ����( )
A�����ˮ����������ǿ���ȼ�յ����ʣ���˿��о��ڲ��ֽ������£�ʹ������Ϊ������Դ
B���跨��̫���ܾ۽��������£�ʹˮ�ֽ��������
C��Ѱ�Ҵ���ʹˮ�ֽ⣬ͬʱ�ͷ�����
D��Ѱ�����⻯ѧ�������ڿ���������Դ���Էֽ�ˮȡ����Դ
��4���ڸ�����һ����̼�ɽ���������ԭΪ������
��C(s)��O2(g)===CO2(g)��H1����393.5 kJ��mol��1
��CO2(g)��C(s)===2CO(g)��H2����172.5 kJ��mol��1
��S(s)��O2(g)===SO2(g)��H3����296.0 kJ��mol��1
��д��CO��SO2��Ӧ���Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ӵ�ʳ���к��е����(KIO3)�����Ե�ⷨ�Ʊ�����أ�ʵ��װ����ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��3I2+6KOH=5KI+KIO3+3H2O��������Һ��������������������������Һ��������������ʼ��⡣����˵������ȷ����
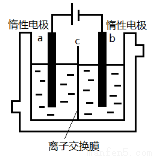
A����������OH-��a����ͨ�����ӽ���Ĥc����b����
B�����ŵ����У�KOH��ҺŨ�Ȼ���С
C����������0.1mol I-�ŵ�ʱ����������6.72LH2
D��a�缫��Ӧʽ��I- -6e-+6OH-=IO3-+3H2O��a������KI����ת��ΪKIO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�յ�����ѧ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣�������и�С�⡣
��1��ϵͳ������ ��
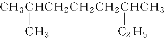
��2��д��֧��ֻ��һ���һ���ʽ����С�������Ľṹ��ʽ�� ��
��3������Ľṹ��ͼ��ʾ��
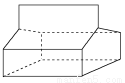
������ķ���ʽΪ________________________��
�����鲻���е�����___ _____��
a����������ˮ b���ܶȴ���ˮ
c��������ˮ�����ӳɷ�Ӧ d�����¡���ѹ��Ϊ����
�������һ�ȴ�����________�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶�������ѡ��ѧ�Ծ��������棩 ���ͣ������
(16��)��ѧ��ѧʵ�飬����ɫ��pH��ֽ�����ڲⶨ��Һ������ԡ��� 25 �棬����Һ��pH=7����ֽ����ɫ����pH<7����ֽ���ɫ����pH>7����ֽ����ɫ����Ҫ��ȷ�ⶨ��Һ��pH������pH�ơ�pH����Ҫͨ���ⶨ��Һ��H+Ũ�����ⶨ��Һ��pH��
��1����֪ˮ�д�������ƽ��H2O  H++OH- ��H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ����� (����ĸ)��
H++OH- ��H>0������ʹƽ�������ƶ�����������Һ�����ԣ�ѡ��ķ����� (����ĸ)��
A����ˮ�м���NaHSO4��Һ
B����ˮ�м���Cu(OH)2����
C������ˮ��100 ��[����c��H+��=1��10-6 mol��L-1]
D����ˮ�м���H2SO4��Һ
��2�������ⶨ100 ���ˮ��pH������ԣ�����pH��ֽ�ⶨ������ֽ�� ɫ������pH�Ʋⶨ����pH 7 (�>����<����=��)����Һ�� ��(��ᡱ������С�)��
��3��ij�жԴ������м�⣬���ָ�����Ҫ��Ⱦ��Ϊ�����������PM2.5(ֱ��С�ڵ���2.5 ��m������������)������Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣����ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±�:
���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
���ݱ��������ж�PM2.5�������Ϊ ��������pH= ��
��4���� ��֪����������NO�ķ�ӦΪN2(g)+O2(g) 2NO(g) ��H>0�����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��
2NO(g) ��H>0�����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ���� ��
�� ����ȼ�Ͳ���ȫȼ��ʱ����CO������������з�Ӧ��ȥCO��2CO(g)��2C(s)+O2(g)����֪�÷�Ӧ�Ħ�H>0�������������ܷ�ʵ�ֵ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ��9���ʼ컯ѧ�Ծ��������棩 ���ͣ������
��12�֣���Ԫ�����ʻ��ã����ڶ�ĺ�������������Ԫ����-2�ۣ���Ҳ���γ�һ�������������۵Ļ����
��1��OF2��һ���ػ�ɫ�ж�������壬�м�ǿ�������ԡ�
��OF2����Ԫ�صĻ��ϼ�Ϊ ��
�ڽ�Fzͨ��ϡ��NaOH��Һ�пɵõ�OF2���ε����ʣ���Ӧ��Ӧ�Ļ�ѧ����ʽΪ________________��
��2������������һ����ɫ����������ԭ������ҵ���ж��ַ����Ʊ�H2O2��
���о�������H2O2�൱�ڶ�Ԫ���ᣬ������һ�����뷽��ʽΪ ����֪������1L��H2O2�൱��48.3 mol����K1��1��67��10 -12������¶���H2O2��c��H����ԼΪ ��д����������Ba��OH��2��Ӧ�Ļ�ѧ����ʽΪ ��
���һ����������Ʊ�����������õķ���������Ҫ���̿�������ͼ��ʾ��д���˹��̵��ܷ�Ӧ����ʽ
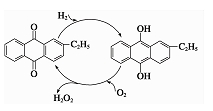
�ۿ����������Ʊ�H2O2��һ�ֻ����Ѻ��͡��������Ʊ�����������ܷ���ʽ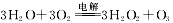 ���������ϵ缫��ӦʽΪ ��
���������ϵ缫��ӦʽΪ ��
��3����Ҳ�����Ԫ���γ�K2O��K2O2��KO2��KO3�����������KO2��һ�ֱ�Na2O2Ч�ʸߵĹ�������д������CO2��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com