
| 实验要求 | 化学试剂 |
| (1)检验酒精中是否有水 | ④ |
| (2)吸收CO中的H2O | ② |
| (3)验证味精中是否有食盐 | ① |
| (4)分离碘水中的碘 | ③ |
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
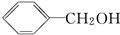 ,B
,B .
.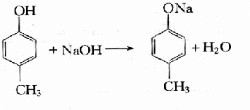 .
. →2
→2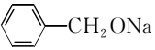 +H2↑.
+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
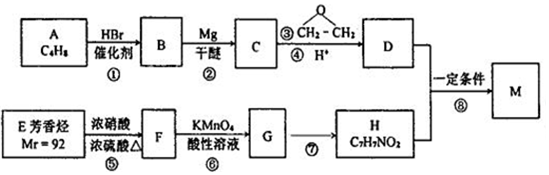

 (苯环上的-NH2易被氧化).
(苯环上的-NH2易被氧化). .
. .
. .
. .
.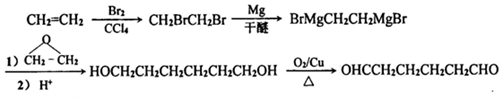 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
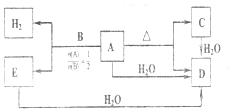
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗铜作阳极 | |
| B. | 用CuSO4溶液作电解液 | |
| C. | 阴极的电极反应式:Cu2++2e-=Cu | |
| D. | 当阳极质量减少ag时,阴极质量增加ag |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,C和D反应生成的化合物的电子式是
,C和D反应生成的化合物的电子式是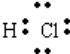 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| C | 向含有酚酞的Na2CO3溶液中加入少量的BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2溶液 | 产生白色沉淀 | 试样已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自来水中加入氯气与污水中加入明矾的原理相同 | |
| B. | 汽油、甘油、花生油均能发生水解反应和氧化反应 | |
| C. | 硫酸铜溶液可用于游泳池的消毒是利用了Cu2+能使蛋白质盐析 | |
| D. | 现代工业生产中的芳香烃来源于石油的催化重整和煤的干馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com