
【题目】如图所示装置可用来制取和观察氢氧化亚铁在空气中被氧化时颜色的变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。
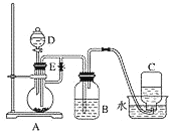
(1)B中盛一定量的氢氧化钠溶液,A中应预先加入的试剂是________,A中反应的离子方程式是_________。
(2)实验开始时就先将止水夹E________(填“打开”或“关闭”),C中收集到气体的主要成分是________。
(3)简述生成氢氧化亚铁的操作过程:__________________。
(4)拔去装置B中的橡皮塞,使空气进入,有关反应的化学方程式是_____________。
【答案】铁屑 Fe+2H+=Fe2++H2↑ 打开 氢气 关闭止水夹E,使硫酸亚铁溶液压入B瓶中进行反应 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
(1)A中应预先盛放固态反应物,铁和稀硫酸发生氧化还原反应生成硫酸亚铁和氢气;
(2)实验开始时,应先打开活塞,使生成的氢气充满整套实验装置中而排出空气,防止氢氧化亚铁被氧化;C中的气体的主要成分为铁和稀硫酸反应生成的氢气;
(3)关闭活塞时,在气体压强的作用下,A中溶液进入B装置中,A中溶液含有硫酸亚铁,可能含有硫酸,硫酸和硫酸亚铁都和氢氧化钠溶液反应;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀。
(1)A中应预先盛放固态反应物铁屑,铁和稀硫酸反应生成硫酸亚铁和氢气,离子反应方程式为:Fe+2H+=Fe2++H2↑;
(2)实验开始时,应先打开活塞,使生成的氢气进入整套实验装置中而排出空气,防止氢氧化亚铁被氧化;氢气不和水反应,所以C中收集的氢气主要是铁和稀硫酸反应生成的氢气;
(3)关闭活塞时,在气体压强的作用下,A中溶液进入B装置中,A中溶液含有硫酸亚铁,硫酸亚铁都和氢氧化钠溶液反应,因此B中产生白色沉淀氢氧化亚铁;
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以看到的现象是:白色沉淀先转化为灰绿色最后转化为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:
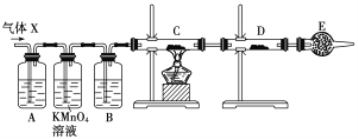
(1)上述反应中生成二氧化硫的化学方程式为______________________________。
(2)乙同学认为还可能产生氢气的理由是__________________________________。
(3)丙同学在安装好装置后,必不可少的一步操作是________________________。
(4)A中加入的试剂可能是_____,作用是__________________________________;B中加入的试剂可能是_____,作用是__________________________________;E中加入的试剂可能是_____,作用是__________________________________。
(5)可以证明气体X中含有氢气的实验现象是:C中:_________________________,D中:_________________________ 。如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?_____ (填“能”或“不能”),原因是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生课外活动小组利用下图所示装置分别做如下实验:
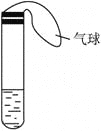
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________溶液;加热时溶液由无色变为红色的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCHO与O2在HAP表面催化氧化的历程示意图如图:(HAP仅为部分结构)
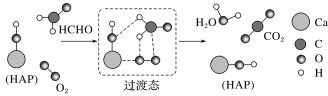
下列说法正确的是( )
A.HAP能提高HCHO的平衡转化率
B.HCHO在反应过程中有C-H键的断裂
C.产物CO2分子中的氧原子全部来自O2
D.该反应可表示为2HCHO+O2![]() CO2+2H2O
CO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品a g(精确到0.1 g),称量时通常使用的主要仪器的名称是_____。
(2)将样品溶解于过量的稀盐酸,过滤并洗涤滤渣。滤液中主要含有________,滤渣为________,溶解、过滤用到的玻璃仪器是________。
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是________________________________________________________________。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是______________________________________________________________。
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是
_______________________________________________________________________,原样品中铝的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表格中的各种情况,可以用右图的曲线表示的是 ( )
反 应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量的氨,在同一容器中 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
C | 在体积可变的恒压容器中,体积比1︰3的N2、H2, | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 molSO2和1 molO2,在相同温度下2SO2+ O2 | SO3物质的量 | 2个大气压 | 10个大气压 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有原子序数依次增大的a、b、c、d四种元素,最外层电子数分别为4、1、x、7,已知c原子的电子层数等于x,d-的电子层结构与Ar元素相同。下列说法错误的是( )
A.元素a与氢形成原子比为1:1的化合物有多种
B.元素b的单质能与水、无水乙醇反应
C.c的简单离子与d-的简单离子最外层电子数和电子层数都不相同
D.元素a与元素d可形成既含有极性共价键又含非极性共价键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
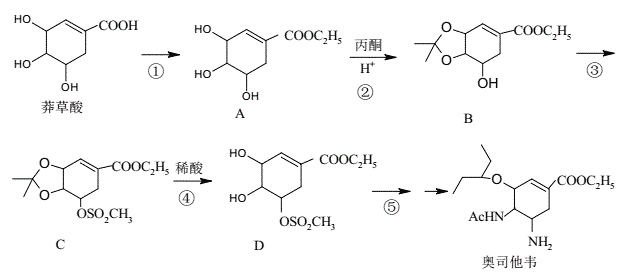
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一。其合成路线如图所示:
回答下列问题:
(1)莽草酸的含氧官能团名称有__;反应③的反应类型__。
(2)反应①的反应试剂和反应条件__。
(3)1molB最多可以消耗___molNaOH溶液。
(4)请写出反应②的化学方程式__。
(5)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有___种。
(6)设计由对甲基苯甲醛制备对醛基苯甲酸![]() 的合成路线__。
的合成路线__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一种丰富的资源,工业上可从海水中提取多种物质,广泛应用于生活、生产、科技等方面。如图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(1)流程图中操作a的名称为____。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①气体A、B是CO2或NH3,则气体A应是_____(填化学式)
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是____。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____。
②操作b是在___氛围中进行,若在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com