

 2NaOH+H2↑+Cl2↑,
2NaOH+H2↑+Cl2↑, 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑; =1.1mol,溶液的质量为100mL×1g/mL+61.6g=161.6g,所以溶液的体积为
=1.1mol,溶液的质量为100mL×1g/mL+61.6g=161.6g,所以溶液的体积为 =
= L,所以氢氧化钾溶液的物质的量浓度为
L,所以氢氧化钾溶液的物质的量浓度为 =10mol/L,故答案为:10mol/L;
=10mol/L,故答案为:10mol/L; 计算出氢氧化钾的物质的量,溶液质量等于溶质质量与溶剂质量之和,利用V=
计算出氢氧化钾的物质的量,溶液质量等于溶质质量与溶剂质量之和,利用V= 计算溶液体积,再根据c=
计算溶液体积,再根据c= 计算氢氧化钾溶液的物质的量浓度;
计算氢氧化钾溶液的物质的量浓度;

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
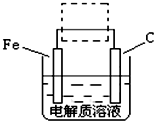 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH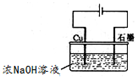 溶液的pH为
溶液的pH为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com