
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=90.7 | C. | 2V2<V3 | D. | α1+α3=0.75 |
分析 甲容器反应物投入1molCO、2molH2与乙容器反应物投入1molCH3OH、丙容器反应物投入2molCH3OH在保持恒温、恒压情况下是等效平衡,平衡时CH3OH的浓度c1=c2 =c3、2V1=2V2=V3、α1+α2=1、α2=α3、a+b能量总变化相当于1molCO、2molH2完全转化成1molCH3OH的能量,即吸放热a+b数值上就等于90.7kJ,c=2b,以此解答该题.
解答 解:A.2molCH3OH相当于2molCO、4molH2,甲和丙相比较,在恒温、恒压下处于相同平衡状态,物质的量增多,体积应增大,达平衡时,浓度相等,则c1=c3,故A错误;
B.甲乙平衡状态相同,不同的是反应的起始方向不同,在此过程中乙吸收的热热量相当于甲完全转化需再放出的热量,故a+b=90.7,故B正确;
C.乙容器反应物投入1molCH3OH、丙容器反应物投入2molCH3OH在保持恒温、恒压情况下是等效平衡,应存在2V2=V3,故C错误;
D.甲乙处于相同的平衡状态,则a1+a2=1,乙、丙平衡状态相同,转化率相同,α2=α3,则α1+α3=1,故D错误;
故选B.
点评 本题主要考查的是化学平衡中的等效平衡问题,等效平衡为在一定条件下(恒温恒容或恒温恒压),对同一可逆反应体系,起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
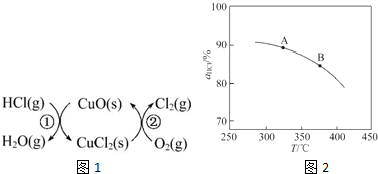
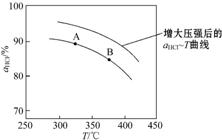 ,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.
,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(Z)>r(Y)>r(M) | |
| B. | Y和M形成的化合物只含有离子键 | |
| C. | 元素非金属性由弱到强的顺序:M、N、X | |
| D. | 电解N和Z形成的化合物可得到Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜全部溶解,且溶液为蓝色,有红棕色气体产生 | |
| B. | 铜部分溶解,且溶液为蓝色,有红棕色气体产生 | |
| C. | 铜全部溶解,且溶液为蓝色,有无色气体产生 | |
| D. | 铜部分溶解,且溶液为蓝色,有无色气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠投入CuSO4溶液中:2Na+Cu2+═2Na++Cu | |
| B. | 过量的CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O═HCO3-+HClO | |
| C. | 向Mg(OH)2悬浊液中滴加四滴0.1mol•L-1FeCl3溶液:3Mg(OH)2(S)+2Fe3+(aq)═2Fe(OH)3(S)+3Mg2+(aq) | |
| D. | 铅酸蓄电池充电时的阳极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “滴水石穿、绳锯木断”不涉及化学变化 | |
| B. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| C. | 明矾净水的原理和“84”消毒液消毒的原理不相同 | |
| D. | 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
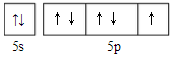 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离的c( H+)=1×l0-13 mol/L的溶液中:K+、Na+、SiO32-、SO42- | |
| B. | 能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- | |
| C. | 甲基橙显黄色的溶液:Na+、CO32-、NO3-、SO32- | |
| D. | 1.0 mol/L的CH3COOH溶液:K+、Fe3+、NO3-、Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com