
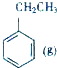
 +CO2(g)?
+CO2(g)?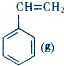 +CO(g)+H2O(g)△H
+CO(g)+H2O(g)△H ?
? +H2(g)△H1=+117.6kJ/mol
+H2(g)△H1=+117.6kJ/mol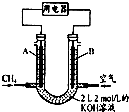
分析 (1)根据盖斯定律结合热化学方程式分析;
(2)①根据浓度熵规则计算Qc是否等于K来计算;
②根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆速率之比等于化学计量数之比(不同物质),各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化;
(3)根据化学反应前后,反应中气体的物质的量之比等于压强之比来回答;
(4)①A为负极、B为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,正极氧气得电子生成氢氧根离子;
②根据苯乙烯和氢氧化钾之间的关系式计算转移电子.
解答 解:(1)方程A+方程B得到: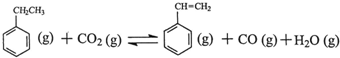 ,所以该反应的反应热为:△H=△H1+△H2=+117.6kJ/mol+41.2kJ/mol
,所以该反应的反应热为:△H=△H1+△H2=+117.6kJ/mol+41.2kJ/mol
=+158.8KJ/mol,
故答案为:+158.8KJ/mol;
(2)①反应 进行到某时刻测得混合物中各组分的物质的量均为1.0mol,即浓度都是0.5mol/L,此时Qc=$\frac{0.{5}^{3}}{0.{5}^{2}}$=0.5=K,所以达到化学平衡状态,
进行到某时刻测得混合物中各组分的物质的量均为1.0mol,即浓度都是0.5mol/L,此时Qc=$\frac{0.{5}^{3}}{0.{5}^{2}}$=0.5=K,所以达到化学平衡状态,
故答案为:是;
②a、都反映的正方向,故a错误;
b、混合气体的平均相对分子质量保持不变,说明气体的物质的量不变反应达平衡状态,故b正确;
c、反应前后体积不变,质量守恒,所以体系的密度始终不变,故不能用密度判断平衡,故c错误;
d、随着反应的进行CO2的体积分数逐渐减小,当CO2的体积分数保持不变,即是平衡状态,故d正确.
故选bd;
(3)已知信息,设乙苯的变化浓度是x,则

初始浓度:4.0 6.0 0 0 0
变化浓度:x x x x x
平衡浓度:4.0-x 6.0-x x x x
则$\frac{4.0-x+6.0-x+3x}{10}$=$\frac{P}{{P}_{0}}$,解得x=$\frac{10(P-{P}_{0})}{{P}_{0}}$,则反应达到平衡时苯乙烯的浓度为 $\frac{10(P-{P}_{0})}{{P}_{0}}$,乙苯的转化率为 $\frac{\frac{10(P-{P}_{0})}{{P}_{0}}}{4}$×100%=$\frac{5(P-{P}_{0})}{2{P}_{0}}$×100%,
故答案为:$\frac{10(P-{P}_{0})}{{P}_{0}}$; $\frac{5(P-{P}_{0})}{2{P}_{0}}$×100%;
(4)①A为负极、B为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,正极氧气得电子生成氢氧根离子,所以B极通入氧气,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:B;O2+2H2O+4e-=4OH-;
②根据C8H8-40e-+56OH-═8CO32-+32H2O知,而10.4g苯乙烯的物质的量为$\frac{10.4}{104}$=0.1mol,所以转移电子的物质的量为0.1×40=4mol,转移电子数为:4NA,故答案为:4NA.
点评 本题综合性较大,涉及化学平衡状态的判断、浓度熵规则、化学平衡的计算等知识,注意知识的归纳和整理是关键,难度不大.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H10的烯烃 | B. | 分子式为C5H12O的醇 | ||
| C. | 分子式为C5H10O2的羧酸 | D. | 分子式为C5H10O2的酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
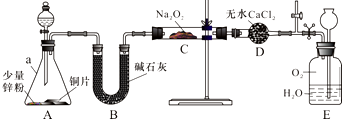 NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.
NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向相同体积,相同pH的两种一元酸中分别加入足量锌粉,测量产生氢气的体积,可以比较两种一元酸的酸性相对较弱 | |
| B. | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至恰好不再有沉淀生成,再向其中滴加Na2S溶液,生成黑色沉淀,说明一种沉淀能转化为另一种溶解度更小的沉淀 | |
| C. | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH,可以比较HClO和CH3COOH的酸性强弱 | |
| D. | 在滴有酚酞Na2CO3溶液中逐滴加入BaCl2溶液,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H10O2的酯类 | B. | 分子式为C5H10的烯烃 | ||
| C. | 分子式为C5H12O的醇类 | D. | 分子式为C5H12的所有化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
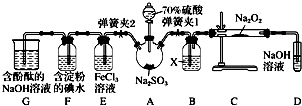
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com