
| 1 |
| 4 |
| A、20 | B、23 | C、30 | D、36 |
| ||
| ||
| 1 |
| 4 |
| ||
| ||
| 1 |
| 4 |
| 2+44 |
| 2 |
| 28+44 |
| 2 |


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
| 选项 | 实验操作或事实 | 实验目的或结论 | ||||
| A | 淡黄色试液
| 说明原溶液中一定含有FeCl3 | ||||
| B | Br2
| 制备少量溶液 | ||||
| C | 无色试液
| 说明原溶液中一定不含钾元素 | ||||
| D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
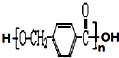
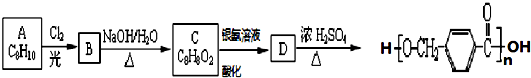
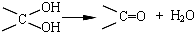
| 无水乙醇 |
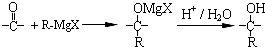
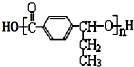 在合成过程中所用的格氏试剂的化学式为
在合成过程中所用的格氏试剂的化学式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量、溶解、蒸发结晶、过滤、洗涤、干燥 |
| B、称量、溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C、溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| D、溶解、蒸发结晶、过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
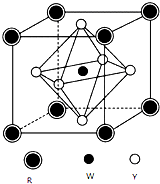 前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得Cl2 |
| B、因海水中含有镁元素,故不需经过化学变化就可以得到镁单质 |
| C、利用蒸馏原理从海水中提取淡水是海水淡化技术发展的新方向 |
| D、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com