
| A. | 常温常压下,0.05NA个CO2分子所占的体积是1.12L | |
| B. | 1mol 氧气所含有的原子数为NA | |
| C. | 常温常压下,32g O2和34g H2S气体分子个数比为1:1 | |
| D. | 11.2L NH3中所含的质子数为5NA |
分析 A.常温常压,Vm≠22.4L/mol;
B.1个氧气分子含有2个氧原子;
C.质量转化为物质的量,分子数目之比等于物质的量之比;
D.气体状况未知,Vm大小未知.
解答 解:A.常温常压,Vm≠22.4L/mol,Vm未知无法计算气体的体积,故A错误;
B.1mol 氧气含有2mol氧原子,所含有的原子数为2NA,故B错误;
C.32gO2的物质的量为$\frac{32g}{32g/mol}$=1mol,34g H2S的物质的量为$\frac{34g}{34g/mol}$=1mol,分子数目之比等于物质的量之比为1:1,故C正确;
D.气体状况未知,Vm大小未知,无法计算氨气的物质的量,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的条件应用,质量换算物质的量计算微粒数的应用,掌握相关公式即可解答.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
| 实验步骤和方法 | 实验现象 |
| ①把6瓶液体分别依次标号A、B、C、D、E、F,然后闻气味 | 只有F没有气味 |
| ②各取少量于试管中,加水稀释 | 只有C、D、E不溶解而浮在水面上 |
| ③分别取少量6种液体于试管中,加新制Cu(OH)并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
| ④各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实现H2→H+H的变化,要放出能量 | |
| B. | 液态水变成气态水要吸收能量 | |
| C. | 金刚石在一定条件变成石墨要吸收能量 | |
| D. | CaO和水反应过程中焓变大于0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
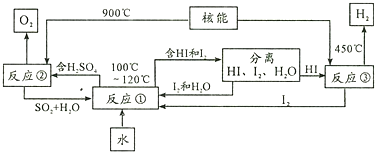
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
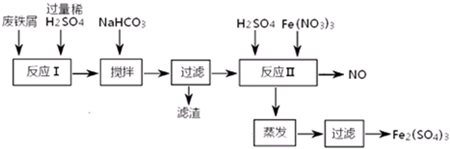
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 氯气和氢氧化钠溶液或石灰乳反应得到的含氯化合物都具有漂白性 | |
| C. | 光导纤维遇强酸会“断路” | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com