
 £©Ė׳ĘŃĢĖį£¬Ī¢ČÜÓŚĖ®£®æÉ×÷ŃŖ¹ÜĄ©ÕÅĄąŅ©Īļ£®Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£©Ė׳ĘŃĢĖį£¬Ī¢ČÜÓŚĖ®£®æÉ×÷ŃŖ¹ÜĄ©ÕÅĄąŅ©Īļ£®Ķź³ÉĻĀĮŠĢīæÕ£ŗ £®ŹŌ¼ĮÅØĻõĖį”¢ÅØĮņĖį£®
£®ŹŌ¼ĮÅØĻõĖį”¢ÅØĮņĖį£®
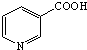
·ÖĪö £Ø1£©3-ßĮą¤¼×Ėįŗ¬ÓŠōČ»ł£¬¾ßÓŠōČĖįŠŌÖŹ£¬NŌ×ÓÓŠ¹Āµē×Ó¶Ō£¬ÄÜÓėĒāĄė×Ó½įŗĻ£¬¾ßÓŠČõ¼īŠŌ£»
£Ø2£©ŃĢĖįµÄŗ¬±½»·µÄĶ¬·ÖŅģ¹¹ĢåĪŖĻõ»ł±½£¬±½ÓėÅØĻõĖį”¢ÅØĮņĖįŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉĻõ»ł±½£»
£Ø3£©ÓÉ3-ßĮą¤¼×ĖįµÄ½į¹¹¼ņŹ½£¬æÉÖŖ3-¼×»łßĮą¤ĪŖ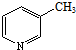 £¬ŌÓ»·Óė±½»·ŠŌÖŹĻąĖĘ£¬ŌŚ¼īŠŌĢõ¼žĻĀÓĆøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµĆµ½
£¬ŌÓ»·Óė±½»·ŠŌÖŹĻąĖĘ£¬ŌŚ¼īŠŌĢõ¼žĻĀÓĆøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµĆµ½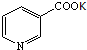 £¬·“Ó¦ŠčŅŖæŲÖĘĪĀ¶ČŌŚ70”ę£¬Ó¦½«øßĆĢĖį¼ŲČÜŅŗ·Ö¶ą“Ī¼ÓČėµ½·“Ó¦ĢåĻµÖŠ£¬¾¹ż¹żĀĖ·ÖĄė£¬ĀĖŅŗÓĆĮņĖįĖį»ÆµĆµ½
£¬·“Ó¦ŠčŅŖæŲÖĘĪĀ¶ČŌŚ70”ę£¬Ó¦½«øßĆĢĖį¼ŲČÜŅŗ·Ö¶ą“Ī¼ÓČėµ½·“Ó¦ĢåĻµÖŠ£¬¾¹ż¹żĀĖ·ÖĄė£¬ĀĖŅŗÓĆĮņĖįĖį»ÆµĆµ½ £¬ÓÉÓŚŃĢĖįĪ¢ČÜÓŚĖ®£¬¹żĀĖæɵĆŃĢĖį£®
£¬ÓÉÓŚŃĢĖįĪ¢ČÜÓŚĖ®£¬¹żĀĖæɵĆŃĢĖį£®
½ā“š ½ā£ŗ£Ø1£©3-ßĮą¤¼×Ėįŗ¬ÓŠōČ»ł£¬¾ßÓŠōČĖįŠŌÖŹ£¬NŌ×ÓÓŠ¹Āµē×Ó¶Ō£¬ÄÜÓėĒāĄė×Ó½įŗĻ£¬¾ßÓŠČõ¼īŠŌ£¬¹ŹŃ”£ŗC£»
£Ø2£©ŃĢĖįµÄŗ¬±½»·µÄĶ¬·ÖŅģ¹¹ĢåĪŖĻõ»ł±½£¬½į¹¹¼ņŹ½ĪŖ £¬±½ÓėÅØĻõĖį”¢ÅØĮņĖįŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉĻõ»ł±½£¬¹Ź“š°øĪŖ£ŗ
£¬±½ÓėÅØĻõĖį”¢ÅØĮņĖįŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉĻõ»ł±½£¬¹Ź“š°øĪŖ£ŗ £»ÅØĻõĖį”¢ÅØĮņĖį£»
£»ÅØĻõĖį”¢ÅØĮņĖį£»
£Ø3£©ÓÉ3-ßĮą¤¼×ĖįµÄ½į¹¹¼ņŹ½£¬æÉÖŖ3-¼×»łßĮą¤ĪŖ £¬ŌÓ»·Óė±½»·ŠŌÖŹĻąĖĘ£¬ŌŚ¼īŠŌĢõ¼žĻĀÓĆøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµĆµ½
£¬ŌÓ»·Óė±½»·ŠŌÖŹĻąĖĘ£¬ŌŚ¼īŠŌĢõ¼žĻĀÓĆøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµĆµ½ £¬ÓÉÓŚ3-¼×»łßĮą¤Ńõ»Æ·Å³öČČĮ棬·“Ó¦ŠčŅŖæŲÖĘĪĀ¶ČŌŚ70”ę£¬Ó¦½«øßĆĢĖį¼ŲČÜŅŗ·Ö¶ą“Ī¼ÓČėµ½·“Ó¦ĢåĻµÖŠ£¬¾¹ż¹żĀĖ·ÖĄė£¬ĀĖŅŗÓĆĮņĖįĖį»ÆµĆµ½
£¬ÓÉÓŚ3-¼×»łßĮą¤Ńõ»Æ·Å³öČČĮ棬·“Ó¦ŠčŅŖæŲÖĘĪĀ¶ČŌŚ70”ę£¬Ó¦½«øßĆĢĖį¼ŲČÜŅŗ·Ö¶ą“Ī¼ÓČėµ½·“Ó¦ĢåĻµÖŠ£¬¾¹ż¹żĀĖ·ÖĄė£¬ĀĖŅŗÓĆĮņĖįĖį»ÆµĆµ½ £¬ÓÉÓŚŃĢĖįĪ¢ČÜÓŚĖ®£¬¹żĀĖæɵĆŃĢĖį£¬“ÖŃĢĖį¾ÕōĮóĢį“æ²Ł×÷ŗóæÉ»ńµĆ“æ¾»µÄŃĢĖį£¬
£¬ÓÉÓŚŃĢĖįĪ¢ČÜÓŚĖ®£¬¹żĀĖæɵĆŃĢĖį£¬“ÖŃĢĖį¾ÕōĮóĢį“æ²Ł×÷ŗóæÉ»ńµĆ“æ¾»µÄŃĢĖį£¬
¹Ź“š°øĪŖ£ŗKMnO4£»H2SO4£»ÕōĮó£»3-¼×»łßĮą¤Ńõ»Æ·Å³öČČĮ棬·“Ó¦ŠčŅŖæŲÖĘĪĀ¶ČŌŚ70”ę£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄŗĻ³É”¢ÓŠ»śĪļµÄ½į¹¹ÓėŠŌÖŹ£¬ĢāÄæÄŚČŻŌŚÖŠŃ§»ł±¾²»Éę¼°£¬ÄŃ¶Č½Ļ“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®µÄµēĄė·½³ĢŹ½£ŗH2O=H++OH- | |
| B£® | pH=7µÄČÜŅŗŅ»¶ØŹĒÖŠŠŌČÜŅŗ | |
| C£® | ÉżøßĪĀ¶Č£¬Ė®µÄµēĄė³Ģ¶ČŌö“ó | |
| D£® | ½«Ļ”“×Ėį¼ÓĖ®Ļ”ŹĶŹ±£¬c£ØH+£©¼õŠ”£¬c£ØOH-£©Ņ²¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
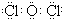 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŹ×ÓŹż | B£® | ÖŠ×ÓŹż | C£® | µē×ÓŹż | D£® | ÖŹĮæŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØĮņĖį | B£® | ¼īŹÆ»Ņ | C£® | ¹żŃõ»ÆÄĘ | D£® | »īŠŌĢæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
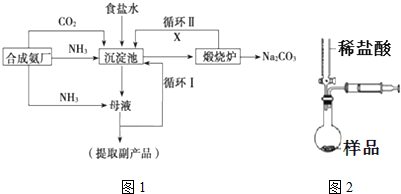
 £¬³Įµķ³ŲÖŠ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+NH3+NaCl+H2OØTNaHCO3”ż+NH4Cl£®
£¬³Įµķ³ŲÖŠ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+NH3+NaCl+H2OØTNaHCO3”ż+NH4Cl£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com